
| A. | 40℃时,0.005mol/LH2SO4溶液的pH为2 | |
| B. | 往氯化铁溶液中滴加氨水来制备氢氧化铁胶体 | |
| C. | 镀锌铁制品镀层受损后,铁制品易生锈 | |
| D. | 已知NaOH溶液和CH3COONH4溶液均显示中性,则两溶液中水的电离程度相同 |
分析 A.pH=-lgc(H+),计算出硫酸中氢离子浓度即可得出其pH;
B.氯化铁与氨水反应生成氢氧化铁沉淀,不会得到氢氧化铁胶体;
C.铁与锌写成的原电池中,锌为负极,则锌优先被腐蚀;
D.醋酸铵中铵根离子和醋酸根离子都发生水解,促进了水的电离.
解答 解:A.40℃时,0.005 mol•L-1 H2SO4溶液中氢离子浓度为0.01mol/L,则该溶液的pH=-lg0.01=2,故A正确;
B.往氯化铁溶液中滴加氨水生成氢氧化铁沉淀,无法获得氢氧化铁胶体,制备氢氧化铁胶体应该将饱和氯化铁溶液加入沸水中,故B错误;
C.镀锌铁制品镀层受损后,二者形成的原电池中,锌为负极,则锌优先被腐蚀,铁制品被保护,故C错误;
D.NaCl溶液为中性,原因是钠离子和氯离子都不水解,而CH3COONH4溶液显中性是由于醋酸根离子与铵根离子的水解程度相等,所以醋酸铵溶液中水的电离程度大于氯化钠溶液,故D错误;
故选A.
点评 本题考查了溶液pH的计算、原电池原理及其应用、盐的水解原理及其应用等知识,题目难度知识,试题知识点较多,充分考查了学生灵活应用基础知识的能力,注意掌握氢氧化铁胶体的制备方法,题目难度中等.


 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 只用淀粉溶液即可检验食盐是否为加碘盐 | |
| B. | 家庭中不宜用铝合金容器长期存放酸性、碱性或咸的食品 | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 用脱硫处理的煤代替原煤作燃料可以有效减少空气中SO2气体的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1某一元弱酸(HA)溶液中:c2(H+)=c(H+)•c(A-)+Kw | |
| B. | 已知Ka(HNO2)=4.6×10-4,Kb(NH3•H2O)=1.8×10-5,可推断NH4NO3溶液呈碱性 | |
| C. | 25℃时,现向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$先增大后减小 | |
| D. | NH4Cl溶液中滴加NaOH溶液至溶液呈中性时,则有c(Na+)>c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
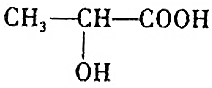 的反应(官能团羟基、羧基,具有醇和酸的性质)
的反应(官能团羟基、羧基,具有醇和酸的性质)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某天然碱样品的组成可能为aNa2CO3•bNaHCO3•cH2O(a、b、c为正整数).为确定其组成,某小组进行如下实验:
某天然碱样品的组成可能为aNa2CO3•bNaHCO3•cH2O(a、b、c为正整数).为确定其组成,某小组进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2和O3 | B. | ${\;}_{1}^{2}$H和${\;}_{1}^{2}$H | ||
| C. | 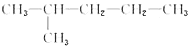 和CH3-CH2-CH2-CH2-CH2-CH3 和CH3-CH2-CH2-CH2-CH2-CH3 | D. | CH3-CH2-CH3和CH3-CH2-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体颜色保持不变 | |
| B. | 体系的平均相对分子质量保持不变 | |
| C. | NO2和SO2的体积比保持不变 | |
| D. | 每消耗1 mol SO2的同时生成1 mol NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com