
下列关于热化学的说法正确的是( )
|
| A. | 需要加热才能发生的反应是吸热反应 |
|
| B. | 等量的金刚石和石墨固体分别完全燃烧,前者放出热量多,说明金刚石更稳定 |
|
| C. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
|
| D. | 由热化学方程式 3H2(g)+N2(g)⇌2NH3(g)△H=﹣92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
考点:
化学能与热能的相互转化.
专题:
化学反应中的能量变化.
分析:
A、吸热反应不一定需要加热才能发生,需要加热才能发生的反应不一定是吸热反应;
B、物质具有的能量越低越稳定;
C、化学反应的反应热=产物的总能量﹣反应物的能量;
D、可逆反应不能进行彻底.
解答:
解:A、吸热反应不一定需要加热才能发生,如氯化铵和氢氧化钡晶体的反应是吸热反应,但是不需要任何条件就能发生,故A错误;
B、等量的金刚石和石墨固体分别完全燃烧,前者放出热量多,则石墨具有能量低,石墨更稳定,故B错误;
C、化学反应的反应热=产物的总能量﹣反应物的总能量,其结果和反应体系的始态和终点状态有关,和路径无关,故C正确;
D、1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放的热量小于92kJ,故D错误.
故选C.
点评:
本题考查学生化学反应的反应热和焓变之间的关系,注意化学反应的吸放热和反应条件之间的关系,难度中等.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
下列微粒的核外电子的表示方法中正确的是( )
|
| A. | 碳原子 |
|
| B. | P原子价电子轨道表示式 |
|
| C. | Cr原子的价电子排布式3d44s1 |
|
| D. | Fe2+价电子排布式3d44s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第八列 |
(1)已知BA5为离子化合物,是由 、 两种微粒构成的(填化学符号).
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,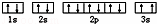 该同学所画的电子排布图违背了 .
该同学所画的电子排布图违背了 .
(4)G位于 族,G3+价电子排布式为 .GE3常温下为固体,熔点282℃,沸点315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断GE3的晶体类型为 .
(5)DE3中心原子的杂化方式为 ,其空间构型为 .
(6)前四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式) ,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
用碳酸钙与1mol/L稀盐酸反应制取二氧化碳,下列措施对化学反应速率几乎没有影响的是( )
|
| A. | 改用浓度为0.5mol/L的稀硫酸 |
|
| B. | 加入更多的碳酸钙 |
|
| C. | 稍微加热,升高反应温度 |
|
| D. | 加入少量醋酸钠晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
3I﹣+S2O82﹣=I3﹣+2SO42﹣的反应速率可以用I3﹣与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,得到的数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I﹣)/mol•L﹣1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82﹣)/mol•L﹣1 | 0.040 | 0.040 | 0.080 | c1 | 0.080 |
| t/s | 88.0 | 44.0 | 22.0 | 22.0 | t2 |
下列说法不正确的是( )
|
| A. | 该实验的目的是探究I﹣与S2O82﹣浓度对反应速率的影响 |
|
| B. | 若在40℃下进行编号③对应浓度的实验,显色时间的范围为<22.0s |
|
| C. | 实验④c1=0.020 mol•L﹣1 |
|
| D. | 实验⑤显色时间t2=11 s |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
|
| A. | 标准状况时,22.4L四氯化碳所含有的分子数为NA |
|
| B. | 34g H2O2中含有的非极性共价键数为 NA |
|
| C. | 碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA |
|
| D. | 将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com