
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:新教材新学案 配合普通高中课程标淮实验教科书 化学② 必修 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:辽宁省东北育才学校高中部2008-2009学年高一下学期第一次月考化学试题 题型:038
有相对原子质量均大于10的A、B两种元素,能形成两种化合物X和Y,已知等物质的量的X和Y形成混合物的密度为相同条件下H2密度的18.5倍,其中X和Y的质量比为15∶22,经测试,X的组成为AB,Y的组成为AnB,通过计算确定A、B两元素名称.(已知A、B的质子数与中子数分别相等)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年宁夏高三上学期第四次月考理综化学试卷(解析版) 题型:填空题
X、Y、Z、L、M、N是六种原子序数依次增大的前四周期元素。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。N的核电荷数比L的核电荷数的3倍多2, 回答下列问题:
(1)X和Y可以形成10电子、14电子、18电子分子,写出X元素质子数和中子数相等的核素的符号 。由X和Y元素组成的14电子分子的电子式为 。
(2)在水溶液中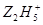 将Fe3+还原为Fe2+,
将Fe3+还原为Fe2+,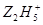 +4Fe3+→4Fe2++……其中化学反应式中的部分物质计量数已给出,该反应的离子方程式为______________________________。
+4Fe3+→4Fe2++……其中化学反应式中的部分物质计量数已给出,该反应的离子方程式为______________________________。
(3)一定条件下,M与TiO2、C(石墨)反应只生成M的氧化物和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知。该反应生成lmol M的氧化物时放出536kJ的热量,其热化学方程式为 。
(4)Z元素的气态氢化物和最高价氧化物对应的水化物化合生成一种盐,该盐的水溶液呈 (填“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序 。
(5)N的低价硫酸盐溶液与过氧化钠反应。若N的低价硫酸盐与过氧化钠的物质的量之比为2:1,且无气体生成,则该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:同步题 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com