
【题目】沙罗特美是一种长效平喘药,其合成的部分路线如下:

(1)F中的含氧官能团名称为____________。
(2)A的名称为____________。
(3)D→E的反应类型为____________,沙罗特美的分子式为____________。
(4)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,写出B的结构简式:____________________。
(5)判断同时满足下列条件的C的同分异构体的数目:_______。(不考虑立体异构)
①分子中含有![]() 结构且只有一个环状结构,与FeCl3发生显色反应;
结构且只有一个环状结构,与FeCl3发生显色反应;
②能与NaHCO3发生反应放出CO2。
③苯环上有且只有三个取代基
(6)请写出以 、(CH3)2C(OCH3)2、CH3NO2为原料制备
、(CH3)2C(OCH3)2、CH3NO2为原料制备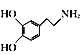 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。_____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。_____________
【答案】醚键、羟基 对羟基苯甲醛 还原反应 C25H37NO4 30种 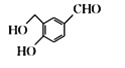

【解析】
(1)由F的结构可知其含有的含氧官能团有:羟基、醚键;
(2)A的名称为对羟基苯甲醛;
(3) D→E将硝基还原成氨基,由沙罗特美的的结构式写出分子式;
(4)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,对比A、C结构,可知A与HCHO发生加成反应生成B,可知B的结构简式为: 。
。
(5)①分子中含有![]() 结构且只有一个环状结构,与FeCl3发生显色反应,说明含有酚羟基;-C3H5有三种结构:-CH=CH-CH3,-CH2CH=CH,
结构且只有一个环状结构,与FeCl3发生显色反应,说明含有酚羟基;-C3H5有三种结构:-CH=CH-CH3,-CH2CH=CH,![]() 。②能与NaHCO3发生反应放出CO2,说明含有羧基。③苯环上有且只有三个取代基,另一个基团为-CH2COOH。三种不同的官能团在苯环上有10种排列,-C3H5有三种结构,故共有30种同分异构。
。②能与NaHCO3发生反应放出CO2,说明含有羧基。③苯环上有且只有三个取代基,另一个基团为-CH2COOH。三种不同的官能团在苯环上有10种排列,-C3H5有三种结构,故共有30种同分异构。
(6)模仿B转化为E的过程、F转化为沙罗特美,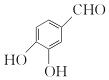 与(CH3)2C(OCH3)2反应生成
与(CH3)2C(OCH3)2反应生成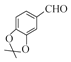 ,然后与CH3NO2发生加成反应生成
,然后与CH3NO2发生加成反应生成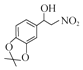 然后发生消去反应生成
然后发生消去反应生成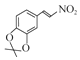 ,再与氢气反应生成
,再与氢气反应生成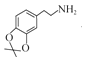 ,最后与氨气作用得到目标物。
,最后与氨气作用得到目标物。
(1)由F的结构可知其含有的含氧官能团有:羟基、醚键;
(2)A的名称为对羟基苯甲醛;
(3) D→E将硝基还原成氨基,D→E的反应类型为还原反应;由沙罗特美的的结构式写出分子式 C25H37NO4;
(4)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,对比A、C结构,可知A与HCHO发生加成反应生成B,可知B的结构简式为: ;
;
(5)①分子中含有![]() 结构且只有一个环状结构,与FeCl3发生显色反应,说明含有酚羟基;-C3H5有三种结构:-CH=CH-CH3,-CH2CH=CH,
结构且只有一个环状结构,与FeCl3发生显色反应,说明含有酚羟基;-C3H5有三种结构:-CH=CH-CH3,-CH2CH=CH,![]() 。②能与NaHCO3发生反应放出CO2,说明含有羧基。③苯环上有且只有三个取代基,另一个基团为-CH2COOH。三种不同的官能团在苯环上有10种排列,-C3H5有三种结构,故共有30种同分异构。
。②能与NaHCO3发生反应放出CO2,说明含有羧基。③苯环上有且只有三个取代基,另一个基团为-CH2COOH。三种不同的官能团在苯环上有10种排列,-C3H5有三种结构,故共有30种同分异构。
(6)模仿B转化为E的过程、F转化为沙罗特美, 与(CH3)2C(OCH3)2反应生成
与(CH3)2C(OCH3)2反应生成 ,然后与CH3NO2发生加成反应生成
,然后与CH3NO2发生加成反应生成 然后发生消去反应生成
然后发生消去反应生成 ,再与氢气反应生成
,再与氢气反应生成 ,最后与氨气作用得到目标物。合成路线流程图为:
,最后与氨气作用得到目标物。合成路线流程图为: .
.


科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)主要用作氯化剂或氯磺化剂,也用于制造医药品、染料、表面活性剂等,熔、沸点分别为-54.1℃和69.2℃。

(1)SO2Cl2中S的化合价为______,SO2Cl2在潮湿空气中发生剧烈反应,散发出具有刺激性和腐蚀性的“发烟”,该反应的化学方程式为____________________。
(2)拟用干燥的SO2和Cl2通入如图装置(省略夹持装置)制取磺酰氯。
①仪器A的名称为___________,通水方向为___________(填 “a→b”或“b→a”),装置B的作用是___________。
②反应装置中的活性炭的作用可能为:______________。
③若SO2和Cl2未经干燥,就通入装置中,也散发出具有刺激性和腐蚀性的“发烟”,该反应的化学方程式为_________。
④滴定法测定磺酰氯的纯度:取1.800g产品,加入到100mL0.5000mol·L1NaOH溶液中加热充分水解,冷却后加蒸馏水准确稀释至250mL,取25mL溶液于锥形瓶中,滴加2滴甲基橙,用0.1000mol·L1标准HCl溶液滴定至终点,重复实验三次取平均值,消耗10.00mL。 达到滴定终点的现象为___________,产品的纯度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A. 原子半径:Na>Mg>O
B. 13C和14C属于同位素
C. 0族元素是同周期中非金属性最强的元素
D. N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X____。
(2)上述实验流程中①②③步均要进行的实验操作是____(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是____________。
(4)按此实验方案得到的溶液3中肯定含有杂质。为了解决这个问题,可以向溶液3中加入适量的________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镓有“电子工业脊梁”的美誉,它与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图所示:

(1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为____________CO2的电子式为_____________________
(2)下列有关Al、Ga的说法不正确的是______
A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga
(3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序_____________
(4)步骤二中不能通入过量的CO2,理由_________________(用离子方程式表示)
(5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+)
①下列有关电解精炼说法正确的是_______
A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.在阴极除了析出高纯度的镓之外,还有H2产生
D.电解后,电解槽底部的阳极泥中只有Cu和Fe
②阴极析出高纯度镓的电极反应式__________________________________
(6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 1molH2和1molI2在加热条件下充分反应,生成HI的分子数为2NA
B. 10g质量分数为46%的乙醇溶液含有的氢原子数目为0.6NA
C. 20mL0.1 mol/LAlCl3溶液中,水解形成Al(OH)3胶体粒子数为0.002NA
D. 0.1molNa2O2和Na2O的混合物中含有的离子总数等于0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解絮凝净水可用如图装置模拟探究,下列叙述正确的是

A. 电子从X极经电解液流入Y极
B. 铝电极表面的反应有:Al -3e-=Al3+,4OH--4e-=O2↑+2H2O
C. Y的电极反应:Pb-2e-+SO42- = PbSO4
D. 电路每通过2mol电子,理论上电解池阴极上有22.4 L H2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.I A族元素均是碱金属元素.
B.第VIA族元素随原子序数的增大,其对应的最简单氢化物的还原性逐渐增强
C.氯的氧化物对应水化物的酸性一定强于碳酸的酸性
D.同周期从左到右主族元素对应单质的熔、沸点依次降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是重要的核工业原料。下列有关
是重要的核工业原料。下列有关![]() 、
、![]() 说法正确的是
说法正确的是
A. ![]() 原子核中含有92个中子 B.
原子核中含有92个中子 B. ![]() 原子核外有143个电子
原子核外有143个电子
C. ![]() 与
与![]() 互为同位素 D.
互为同位素 D. ![]() 与
与![]() 互为同素异形体
互为同素异形体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com