
| A、饱和纯碱(Na2CO3)溶液中:c(Na+)=2c(CO32-) |
| B、pH=4的醋酸中:c(H+)=1.0×10-4mol?L-1 |
| C、0.10mol/L醋酸钠溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| D、pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |


科目:高中化学 来源: 题型:
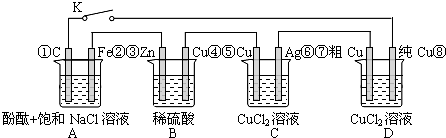
| A、当K闭合时,A装置发生吸氧腐蚀,在电路中做电源 |
| B、当K断开时,B装置锌片溶解,有氢气产生 |
| C、当K闭合后,整个电路中电子的流动方向为①→⑧;⑦→⑥;⑤→④;③→② |
| D、当K闭合后,A、B装置中pH变大,C、D装置中pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| 制备氢氧化铝 | 加热碳酸氢钠固体 | 排空气法收集NH3、Cl2、NO、CO2等气体 | 配制100mL 0.1000mol?L-1 NaOH溶液 |
 |
 |
 |
 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从安全的角度考虑,金属钠着火时,应立即用水将其扑灭 |
| B、氢氧化铁溶胶、乙酸与乙醇的混合液、含PM2.5的大气均为胶体 |
| C、纤维素在人体内可发生水解反应,故可做人类的营养物质 |
| D、石英可用于生产光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、央视曝光“毒胶囊”事件,主要是其中重金属含量超标,重金属对人体危害主要是使蛋白质变性 |
| B、大量焚烧田间秸秆会产生雾霾,“雾”和“霾”的分散质微粒相同 |
| C、人体内没有能使纤维素水解成葡萄糖的酶,因此纤维素不能作为人类的营养食物 |
| D、针对H7N9流感的扩散情况,常选用含氯消毒剂、双氧水等物质进行消毒预防 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用萃取的方法可将汽油和煤油进行分离 |
| B、加过量稀盐酸后过滤,可除去混在铜粉中的少量镁粉和铝粉 |
| C、用溶解、过滤的方法可分离硝酸钾和氯化钠固体混合物 |
| D、将混有氢气的氧气通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2 | ||
| B、钠与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+ | ||
| C、向硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3 | ||
D、将铜片放入足量稀硝酸中:3Cu+8H++2NO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com