
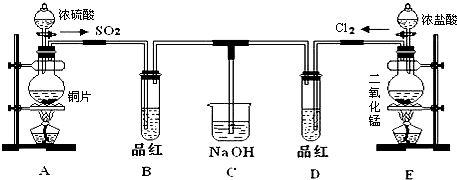
分析 (1)根据装置图可知,A中是铜与浓硫酸反应生成二氧化硫、硫酸铜和水,在该反应中浓硫酸既有氧化性又有酸性;
(2)实验室用装置E中二氧化锰与浓盐酸加热制备Cl2,同时生成氯化锰和水,根据化合价的变化可知,该反应中氯化氢中的氯从-1价变为0价,据此答题;
(3)①根据装置图可知,装置A和E中,常用于萃取操作的仪器是分液漏斗;
②二氧化硫漂白后的物质具有不稳定性,而氯气的漂白具有不可逆性;
(4)SO2和Cl2按1:1通入,SO2和Cl2恰好反应,二者反应生成H2SO4和HCl;
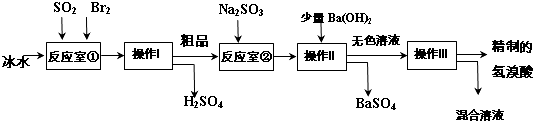
(5)Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,反应室1中发生反应:SO2+Br2+2H2O=H2SO4+2HBr,Br2氧化SO2放出很多热量,液溴、氢溴酸易挥发,反应室①使用冰水降低温度,防止Br2和HBr挥发,操作I是将互溶的硫酸、氢溴酸分离,而氢溴酸易挥发,应采取蒸馏进行分离.粗品中可能含有挥发出的Br2,加入Na2SO3,除去粗品中未反应完的溴,再加入氢氧化钡溶液,使反应生成SO42- 转化硫酸钡沉淀,再进行过滤分离,无色溶液中含有HBr及NaBr,再蒸馏得到精制的氢溴酸,④A用KSCN溶液检验Fe3+,滴加KSCN溶液,溶液变成血红色;B由工艺流程可知,溶液中可能含有Br2,可以用CCl4萃取方法检验.
解答 解:(1)根据装置图可知,A中是铜与浓硫酸反应生成二氧化硫、硫酸铜和水,反应方程式为Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,在该反应中浓硫酸既有氧化性又有酸性,
故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;既有氧化性又有酸性;
(2)实验室用装置E中二氧化锰与浓盐酸加热制备Cl2,同时生成氯化锰和水,反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,根据化合价的变化可知,该反应中氯化氢中的氯从-1价变为0价,所以该反应中的还原剂是HCl,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;HCl;
(3)①根据装置图可知,装置A和E中,常用于萃取操作的仪器是分液漏斗,
故答案为:分液漏斗;
②二氧化硫漂白后的物质具有不稳定性,加热时又能变为红色,而氯气的漂白具有不可逆性,加热也不能恢复红色,
故答案为:褪色的品红恢复红色;无明显现象;
(4)SO2和Cl2按1:1通入,SO2和Cl2恰好反应,二者反应生成H2SO4和HCl,发生Cl2+SO2+2H2O=2HCl+H2SO4,不再具有漂白性,
故答案为:Cl2+SO2+2H2O=2HCl+H2SO4;
(5)①Br2氧化SO2放出很多热量,液溴、氢溴酸易挥发,反应室①使用冰水降低温度,防止Br2和HBr挥发,
故答案为:防止Br2和HBr挥发;
②操作I是将互溶的硫酸、氢溴酸分离,而氢溴酸易挥发,应采取蒸馏进行分离;操作Ⅱ分离固体与液体,应是过滤,
故答案为:蒸馏;过滤;
③粗品中可能含有挥发出的Br2,加入Na2SO3,还原除去粗品中的Br2,
故答案为:还原除去粗品中的Br2;
④A用KSCN溶液检验Fe3+:取少许溶液滴加KSCN溶液,溶液变成血红色,说明氢溴酸呈淡黄色是因为含Fe3+,
故答案为:KSCN溶液;溶液变成血红色;
B由工艺流程可知,溶液中可能溶解了少量Br2,可以用CCl4萃取方法检验:加入CCl4进行萃取,若观察CCl4中有橙红色液体出现,则可证明,
故答案为:溶解了少量Br2;加入CCl4进行萃取,若观察CCl4中有橙红色液体出现,则可证明.
点评 本题考查氯气和二氧化碳漂白性的对比实验,题目难度中等,本题注意二者的性质的异同,特别是漂白原理的不同.本题以制备氢溴酸为载体,考查学生对工艺流程的理解、物质的分离提纯等基本操作、离子检验、物质性质等,难度中等,是对知识的综合运用,需学生具有扎实的基础知识与灵活运用知识解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 氨基酸、淀粉均属于高分子化合物 | |
| B. | 乙醇不能发生取代反应 | |
| C. | 苯能使溴水褪色是因为发生了加成反应 | |
| D. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
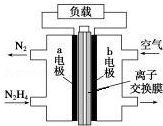 液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列 关于该电池的叙述错误的是( )
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列 关于该电池的叙述错误的是( )| A. | b 极发生还原反应 | |
| B. | a 极的反应式为 N2H4-4e-═N2↑+4H+ | |
| C. | 放电时,电流从 b 极经过负载流向 a 极 | |
| D. | 其中的离子交换膜需选用阴离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘化钾--加碘盐 | B. | 氧化铝--耐火材料 | ||
| C. | 铁碳合金--碳素钢 | D. | 硅酸盐--普通玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何可逆反应都有一定的限度 | |
| B. | 对于反应2SO2(g)+O2(g)?2SO3(g)只有达到限度时才有2v(O2)=v(SO3) | |
| C. | 对于反应2SO2(g)+O2(g)?2SO3(g)达到限度时,增大容器容积能减小正反应速率 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Cl-、NO3-、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | K+、SO42-、Cu2+、NO3- | D. | NH4+、OH-、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com