
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 结果分析 |
| 步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解, 滴加足量稀硝酸酸化,再滴加几滴AgNO3溶液 滴加足量稀硝酸酸化,再滴加几滴AgNO3溶液 . |
有白色沉淀生成,说明产品中含有NaCl. |
| 步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1. 再向已变无色的溶液中滴加几滴甲基橙,继续用该盐酸滴定至溶液由黄色变为橙色 再向已变无色的溶液中滴加几滴甲基橙,继续用该盐酸滴定至溶液由黄色变为橙色 ,记录消耗盐酸的体积V2. |
V2>V1 V2>V1 ,说明产品中含有NaHCO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:
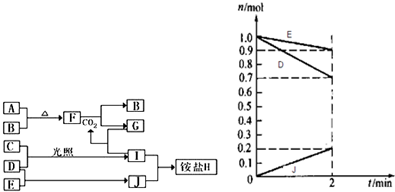
 2NH3
2NH3 2NH3
2NH3查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无明显现象 |
| ② | B+D | 有无色无味气体放出 |
| ③ | C+B | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com