
 ij��ѧС���������������������װ�ã���ͼ�����Ի������Ʊ�����ϩ
ij��ѧС���������������������װ�ã���ͼ�����Ի������Ʊ�����ϩ
| �ܶȣ�g/cm3�� | �۵� ���棩 | �е� ���棩 | �ܽ��� | |
| ���Ѵ� | 0.96 | 25 | 161 | ������ˮ |
| ����ϩ | 0.81 | -103 | 83 | ������ˮ |
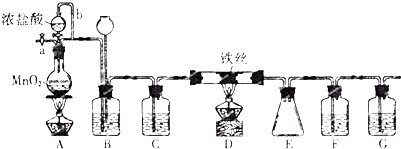
���� ��1���ٸ���ʵ��������ϩ��֪������װ��A�����Ƭ�������Ƿ�ֹ���У�����B�Ƚϳ���������������ĽӴ�������������ǵ����ͽ����ɵ�������������������
�ڱ�ˮԡ��Ŀ���ǽ��ͻ���ϩ�������¶ȣ�ʹ��Һ����
��2������ϩ�������Ȼ�����Һ�����ܶȱ�ˮС���ֲ��ϩ���ϲ㣬���ڷ�Һ��ϩ��Ʒ�л�������������ͻ����������룺�Ʊ����������ᴿ����ʱ��c��Na2CO3��Һ��ϴ�ӿɳ�ȥ�ᣮ
��� �⣺��1���ٸ���ʵ��������ϩ��֪������װ��A�����Ƭ�������Ƿ�ֹ���У�����B�Ƚϳ���������������ĽӴ�������������ǵ����ͽ����ɵ�������������������
�ʴ�Ϊ����ֹ���У�����������
�ڱ�ˮԡ��Ŀ���ǽ��ͻ���ϩ�������¶ȣ�ʹ��Һ����
�ʴ�Ϊ����һ����ȴ����ֹ����ϩ�ӷ���
��2������ϩ�����࣬�������Ȼ�����Һ�����ܶȱ�ˮС�������á��ֲ��ϩ���ϲ㣻����ϩ�к���̼̼˫�������Ա�KMnO4��Һ������ϡH2SO4���ܳ�ȥ�������������µ��������ʣ�ֻ��Na2CO3��Һ�������뻷��ϩ��Ӧ���������������ʷ�Ӧ����ѡ��
�ʴ�Ϊ���ϣ�c��
���� �������л��ϳ�Ϊ���壬�ۺϿ����˻���ϩ���Ʊ���������ѧ������֪ʶ����������Ŀ�Ѷ��еȣ�ע�����ʵ��ԭ���ͷ������ر���ʵ��Ļ���������ѧϰ��ע����ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���������磬���ˮ�Ƿǵ���� | |
| B�� | ���κ��¶��£���ˮ��pH������7 | |
| C�� | ��ˮ�м����ƣ���Һ��$\frac{{K}_{w}}{c��O{H}^{-}��}$��С | |
| D�� | ��ˮ�м�����ᣬc��H+����ˮ�ĵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
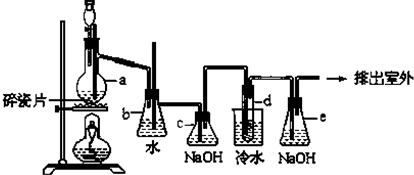
 ��������������ȡȾ�Ϻ�һЩҩ�����Ҫ�м��壬���ɱ�����Ũ���ᣨHO-SO3H���ǻ��õ���ʵ���ҿ�������ͼװ�úϳɶ���������
��������������ȡȾ�Ϻ�һЩҩ�����Ҫ�м��壬���ɱ�����Ũ���ᣨHO-SO3H���ǻ��õ���ʵ���ҿ�������ͼװ�úϳɶ���������
| ���� | ���������� | |
| �۵� | -6.3�� | 288�� |
| �е� | 184�� | ��300�濪ʼ�ֽ�̿���� |
| ˮ���� | ����ˮ | ������ˮ��������ˮ |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| 25��ʱ | pHֵ |
| ����H2S��Һ | 3.9 |
| SnS������ȫ | 1.6 |
| FeS��ʼ���� | 3.0 |
| FeS������ȫ | 5.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ҵ�ϳ����ú����ˮ����Na2S2O3•5H2O��ijС��ͬѧ������װ�ã���ȥ���ּг��������������Ѽ��飩ģ���������̣�ʵ�鲽���ǣ�����C����ƿ����Na2S��Na2SO3�����Һ������A����ƿ�μ�ŨH2SO4����Na2S��Na2SO3��ȫ���ĺ���C�л�����Һ���ᾧ���õ���Ʒ��
��ҵ�ϳ����ú����ˮ����Na2S2O3•5H2O��ijС��ͬѧ������װ�ã���ȥ���ּг��������������Ѽ��飩ģ���������̣�ʵ�鲽���ǣ�����C����ƿ����Na2S��Na2SO3�����Һ������A����ƿ�μ�ŨH2SO4����Na2S��Na2SO3��ȫ���ĺ���C�л�����Һ���ᾧ���õ���Ʒ��| ���� | ʵ����� | ʵ������ |
| I | ȡ������Ʒ���ϡ��Һ���μ�����BaCl2��Һ | �а�ɫ�������� |
| II | ���ˣ�������ˮϴ�ӳ�����������м��� ����ϡ���� | ����δ��ȫ�ܽ⣬���д̼�����ζ��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com