
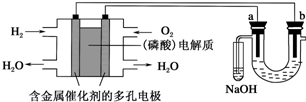
| A. | 电池工作时,正极反应式为O2+2H2O+4e-═4OH- | |
| B. | 电解时,a电极周围首先放电的是Cl-,而不是Br- | |
| C. | 电解时,电子流动路径是:负极-→外电路-→阴极-→溶液-→阳极-→正极 | |
| D. | 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.02 g H2 |
分析 A、氢氧燃料电池中,正极上放电的是氧气;
B、还原性:Br->Cl-,还原性强的离子在阳极先放电;
C、电子在导线中移动,不能在溶液中移动;
D、燃料电池和电解池中转移的电子数是相等的.
解答 解:A、氢氧燃料电池中,正极上放电的是氧气,在酸性电解质环境下,电极反应式为:O2+4H++4e-═2H2O,故A错误;
B、还原性强的离子在阳极先放电,因为还原性:Br->Cl-,所以电解时a电极周围首先放电的是Br-而不是Cl-,故B错误;
C、电子在导线中移动,不能在溶液中移动,则电子流动路径是:负极-→外电路-→阴,阳极-→正极,故C错误;
D、燃料电池和电解池中转移的电子数是相等的,当电池中消耗0.02gH2,根据电极反应:H2→2H++2e-,所以转移电子0.02mol,b极的电极反应为:2H++2e-→H2,转移电子0.02mol,会产生0.02gH2,故正确.
故选D.
点评 本题考查了原电池和电解池,明确原电池和电解池原理是解本题关键,知道离子的放电顺序,易错选项是C,注意电子不进入电解质溶液,溶液中阴阳离子定向移动而形成电流,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
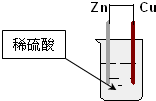
| A. | 铜片表面有气泡产生 | B. | 负极反应为:Cu-2e-=Cu2+ | ||
| C. | 锌为负极,铜为正极 | D. | 电子通过锌片经导线流向铜片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应和复分解反应不可能是氧化还原反应 | |
| B. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| C. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| D. | 在氧化还原反应中肯定有一种元素被氧化,另一种元素被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
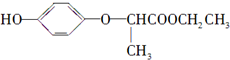 下列有关HPE的说法正确的是( )
下列有关HPE的说法正确的是( )| A. | 1 mol HPE最多可和2 mol NaOH反应 | |
| B. | HPE不能跟浓溴水反应 | |
| C. | HPE不能发生加成反应 | |
| D. | HPE在核磁共振氢谱中有6个峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1mol水和1molH2的体积都约是22.4L | |
| B. | 2gH2和44gCO2的体积相等 | |
| C. | 1mol某气体的体积为22.4L,则该气体一定处于标准状况 | |
| D. | 在标准状况下,1gH2和11.2LO2的物质的量相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com