
��ϡ������п��Ӧ��ȡ������ʵ���У�̽����������ͭ
��Һ�����������������ʵ�Ӱ�졣ʵ����Zn�������ҿ�����С��ͬ����������ͭ��Һ����0һ4. 0mL����
����Һ�����Ϊ100. 0mL����¼�����ͬ���(336 mL,)����������ʱ�䣬ʵ������ͼ��ʾ(���������ת
��Ϊ�����)����ͼ����������˵������ȷ����

A����������ͭ��Һ����������ڸ����ռ�����
B��a ,c�����Ӧ�����������������
C��b���Ӧ�ķ�Ӧ����Ϊv( H2SO4)��1.0x10-3mol��L -1 ��s-1
D��d��û�й���ԭ��أ���Ӧ���ʼ���
 ������ѧ���̲���ȫ���ϵ�д�
������ѧ���̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�������ֵ�����������в���ȷ���ǣ�
A�����³�ѹ�£�1mol����-CH3)���еĵ�����Ϊ9NA
B��1 mol FeCl3��ˮ��ȫ��Ӧת��Ϊ������������������ӵ���ĿС��NA
C������£�2.24LHF�к��еĵ�����ΪNA
D��1 mol ���ɰ(SiC)�к���4NA̼���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ�Ӧ������д��ȷ���� �� ��
A. H2O + H2O 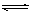 H3O+ + OH�� B. CO32��+ 2H2O
H3O+ + OH�� B. CO32��+ 2H2O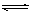 H2CO3 + 2OH��
H2CO3 + 2OH��
C. Ca(OH)2 + 2H+ 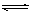 Ca2+ + 2H2O D. Al3++3H2O == Al(OH)3�� + 3H+
Ca2+ + 2H2O D. Al3++3H2O == Al(OH)3�� + 3H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
þ���������Ͻ��������Ӳ��ϡ�þ�Ͻ𱻹���Ϊ��21������ɫ�������Ͳ��ϡ����ɹ㷺�����ں��պ��졢������10��������ְ�þ��Ͷ�뵽ʢ������ij��������У�����H2��������ͼ��ʾ�������������жԲ���H2����û��Ӱ�����(����)
A����Һ���¶� B��þ���ı����
C��Cl����Ũ�� D��H����Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���� (����)
�ٲμӷ�Ӧ�����ʵ�������Ӱ�컯ѧ��Ӧ���ʵ���Ҫ����
�� ����Ӱ��ijЩ��ѧ��Ӧ���ʵ��������֮һ���۾�����ѧ��Ӧ���ʵ���Ҫ������Ũ�ȡ�
����Ӱ��ijЩ��ѧ��Ӧ���ʵ��������֮һ���۾�����ѧ��Ӧ���ʵ���Ҫ������Ũ�ȡ�
�ܲ���ʲô��Ӧ������Ũ�ȡ����ȡ���ѹ��ʹ�ô��������Լӿ췴Ӧ����
A���٢� B���ڢ� C���ۢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£�N2O�ֽ�IJ���ʵ���������£�
| ��Ӧʱ��/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| c(N2O)/mol/L | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
��ͼ����ȷ��ʾ�÷�Ӧ�й��������仯���ɵ���
(ע��ͼ�а�˥��ָ��һŨ��N2O����һ��ʱ�������Ӧʱ�䣬c1��c2����ʾN2O��ʼŨ����c1��c2)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���¶��£���1 mol N2O4�������Ϊ1 L���ܱ������У���Ӧ3 s
��NO2�����ʵ���Ϊ0��6 mol����0��3 s�ڵ�ƽ����Ӧ����v(N2O4)��________mol��L��1��s��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ȫ�к�50ml���ʵ���Ũ��Ϊ2mol/LnaOH
��Һ��ҪH2SO4�������Ƕ��٣�������ЩH2SO4����ˮ���500ml��Һ����H2SO4�����ʵ���Ũ���Ƕ���?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��H2(g)��Br2(g)��������ܱ������������·�����Ӧ��H2(g)��Br2(g)===2HBr(g)����H��0��ƽ��ʱBr2(g)
��ת����Ϊa������ʼ������ͬ������ �½���������Ӧ��ƽ��ʱBr2(g)��ת����Ϊb��a��b�Ĺ�ϵ�� (����)
�½���������Ӧ��ƽ��ʱBr2(g)��ת����Ϊb��a��b�Ĺ�ϵ�� (����)
A��a��b B.a��b C��a��b D����ȷ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com