

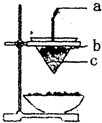
| A. | 加热时,①上部汇聚了固体碘,说明碘的热稳定性较差 | |
| B. | 加热时,②、③中的溶液为无色,冷却后又都变红 | |
| C. | ④中,浸泡在热水中的容器内气体颜色变浅,浸泡在冰水中的容器内气体颜色变深 | |
| D. | 四个“封管实验”中不是都有可逆反应发生 |
分析 A.碘单质易升华,属于碘单质的物理性质,不能据此判断碘的热稳定性;
B.氨气使酚酞溶液变红,二氧化硫能够使品红溶液褪色;
C.二氧化氮转化成四氧化二氮的反应为放热反应,升高温度平衡向着逆向移动;
D.可逆反应,须在同等条件下,既能向正反应进行,又能向逆反应进行.
解答 解:A.加热时,①上部汇集了固体碘单质,说明碘发生了升华现象,为其物理性质,不能说明碘单质的热稳定性较差,故A错误;
B.②中氨水显碱性,使酚酞变红,加热时,氨气逸出,冷却后,氨气又和水反应,变成红色,二氧化硫与品红显无色,加热后二氧化硫逸出,显红色,二者现象不同,故B错误;
C.2NO2(g)?N2O4(g)△H=-92.4kJ/mol,正反应为放热反应,升高温度平衡向逆反应方向移动,则颜色变深,④中浸泡在热水中的容器内气体颜色变深,反之变浅,所以浸泡在冰水中的容器内气体颜色变浅,故C错误;
D.①中碘的升华为物理变化;②中一水合氨的电离为可逆反应;③中亚硫酸的电离为可逆过程,④中二氧化氮与四氧化二氮的转化为可逆反应,所以四个“封管实验”中不是都有可逆反应发生,故D正确;
故选D.
点评 本题考查化学实验方案的评价,涉及可逆反应、漂白性、平衡移动的因素、碘单质的性质等知识,注重基础知识的考查和实验原理,题目难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸只起到吸水作用,不参与反应 | |
| B. | 反应体系中含18O的分子有2种 | |
| C. | 乙酸乙酯中还有18O 原子 | |
| D. | 反应一段时间后乙醇中含有18O原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①②③ | C. | ②③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属熔点的高低 | B. | 金属阳离子得电子的能力 | ||
| C. | 金属在自然界的存在形式 | D. | 金属元素在地壳中的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2,2ClO-+CO2+H2O═2HClO+CO32- | |
| B. | 向Fe(NO3)2和NaBr混合溶液中滴加稀盐酸:6Br-+8H++2NO3-═3Br2+2NO↑+4H2O | |
| C. | 在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7,Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 双氧水使酸性KMnO4溶液褪色:2MnO4-+5H2O2═2Mn2++5O2↑+6OH-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com