
| A. | NaOH | B. | 浓H2SO4 | C. | Na2O2 | D. | 浓盐酸 |
分析 A.氢氧化钠能够吸收空气中的水分并与二氧化碳反应;
B.浓硫酸具有吸水性;
C.过氧化钠能够与空气中的水、二氧化碳反应;
D.浓盐酸具有易挥发性.
解答 解:A.氢氧化钠能够吸收空气中的水分并与二氧化碳反应,固体质量增加,故A不选;
B.浓硫酸具有吸水性,吸收空气中的水分而质量增加,故B不选;
C.过氧化钠与空气中水蒸气、二氧化碳反应,反应方程式为2Na2O2+2H2O═4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2↑,根据方程式可知反应后固体质量增大,故C不选;
D.浓盐酸具有挥发性,氯化氢挥发,溶质的质量减少,溶液的质量减小,故D选;
故选:D.
点评 本题考查了元素化合物知识,熟悉相关物质的化学性质是解题关键,注意浓硫酸吸水性与浓盐酸的挥发性,题目难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LSO3所含电子数约为40NA | |
| B. | 0.5molNH4HSO4晶体中,含有H+数目约为0.5NA | |
| C. | 48gO2,O3混合气体含有的氧原子数为3NA | |
| D. | 1molCl2作为氧化剂得到的电子数一定为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
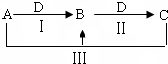 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去).
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y元素为Na元素 | B. | X只能位于第3周期 | ||
| C. | a+n-b+m=10或16 | D. | Y不可能位于第2周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 是离子化合物,含有离子键和共价键 | |
| B. | 电子式是 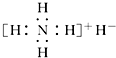 | |
| C. | 与水反应时,它既是还原剂又是氧化剂 | |
| D. | 固体投入少量的水中,有两种气体产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com