
| A. | 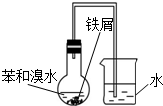 实验室制取溴苯 | B. | 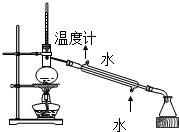 石油的分馏实验 | ||
| C. | 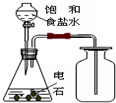 实验室制取乙炔并收集 | D. |  利用酒精萃取碘水中的I2单质 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
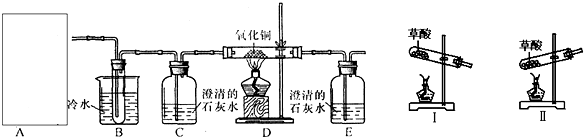
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2015年10月5日,中国著名药学家屠呦呦获得诺贝尔奖生理学或医学奖,获奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.从植物黄花蒿茎 叶中提取的,其结构简式如图,下列说法不正确的是( )
2015年10月5日,中国著名药学家屠呦呦获得诺贝尔奖生理学或医学奖,获奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.从植物黄花蒿茎 叶中提取的,其结构简式如图,下列说法不正确的是( )| A. | 它的分子式为C15H2205 | |
| B. | 青蒿素易发生加成反应和氧化反应 | |
| C. | 青蒿素在碱性条件下易发生水解反应 | |
| D. | 它在常见有机溶剂中的溶解度大于在水中的溶解度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | 铜和稀硝酸反应:Cu+2H+═H2↑+Cu2+ | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Q>W | |
| B. | Q和W可形成原子个数比为1:1和2:1的化合物 | |
| C. | X 与W能形成两种常见的化合物 | |
| D. | Y单质既能与盐酸反应,又能与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时MgxMo3S4只发生还原反应 | |
| B. | 放电时Mo3S4只发生氧化反应 | |
| C. | 充电时阳极反应式为 Mo3S42x--2xe-=Mo3S4 | |
| D. | 放电时负极反应式为xMg=xMg2+-2xe- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com