


科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
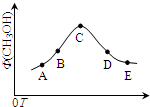 火力发电厂释放出的大量氧化物(NOx)、SO2、CO2会对环境造成污染.对这些废气进行脱硝、脱碳和脱硫处理,可达到节能减排、废物利用等目的.
火力发电厂释放出的大量氧化物(NOx)、SO2、CO2会对环境造成污染.对这些废气进行脱硝、脱碳和脱硫处理,可达到节能减排、废物利用等目的.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈 |
| ② | 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与葡萄糖互为同分异构体 |
| B、可以与银氨溶液作用形成银镜 |
| C、与葡萄糖互为同系物 |
| D、可以使石蕊试液变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓度均为0.02 mol?L-1的AgNO3和CH3COONa溶液混合一定产生CH3COOAg沉淀 |
| B、将0.1 mol/LAgNO3溶液逐滴加入到0.001mol/LKCl和0.001mol/LK2S溶液中,先产生AgCl沉淀 |
| C、要使Mg2+浓度为0.12 mol?L-1的溶液中产生Mg(OH)2的沉淀,溶液的pH≥9 |
| D、向0.1mol/L AgNO3溶液中滴加0.1mol/LNaCl溶液至不再有白色沉淀生成,再向其中滴加0.1mol/L的Na2S溶液,白色沉淀转化为黑色沉淀.则其离子方程式为:2Ag++S2-(aq)?Ag2S(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgI比AgCl稳定 |
| B、碘氧化性比氯弱 |
| C、I-的还原性比Cl-强 |
| D、溶度积Ksp(AgI)<Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率降低 |
| C、平衡向正反应方向移动 |
| D、C的质量分数增加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com