
科目:高中化学 来源: 题型:选择题
| A. | .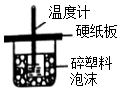 装置用于中和热的测定 | |
| B. | 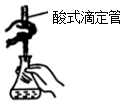 装置用于高锰酸钾溶液滴定草酸 | |
| C. | 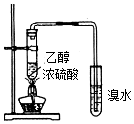 装置用于制取乙烯并验证乙烯的性质 | |
| D. | 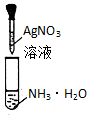 装置用于配制银氨溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
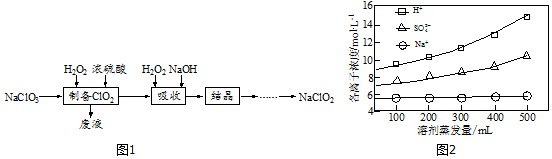
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3 | B. | NaAl(OH)2CO3 | C. | Mg(OH)2 | D. | BaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3:2:1 | |
| B. | n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为$\frac{35.5m}{n}$ | |
| C. | 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 | |
| D. | 5.6 g CO和22.4 L CO2中含有的碳原子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
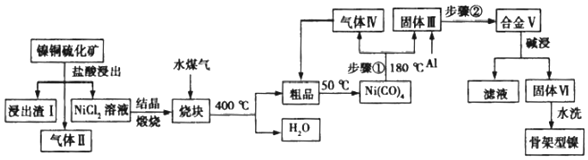
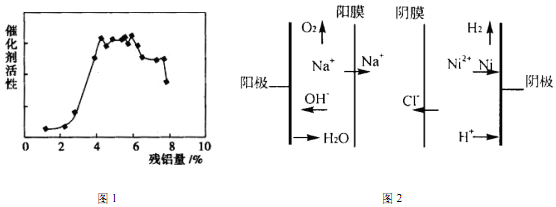
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 ,该反应的反应类型为加成反应
,该反应的反应类型为加成反应 .
. .此空多余
.此空多余 可用于合成有机高分子色素,根据Claisen缩合反应,设计以甲醛和乙醛为原料合成聚丙烯醛的路线.合成路线流程图示例如下:H2C═CH2$→_{催化剂加热}^{HBr}$CH3CH2Br$→_{加热}^{NaOH溶液}$CH3CH2OH.HCHO+CH3CHO$→_{△}^{NaOH(aq)}$nCH2═CHCHO$→_{△}^{催化剂}$
可用于合成有机高分子色素,根据Claisen缩合反应,设计以甲醛和乙醛为原料合成聚丙烯醛的路线.合成路线流程图示例如下:H2C═CH2$→_{催化剂加热}^{HBr}$CH3CH2Br$→_{加热}^{NaOH溶液}$CH3CH2OH.HCHO+CH3CHO$→_{△}^{NaOH(aq)}$nCH2═CHCHO$→_{△}^{催化剂}$ .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com