
分析 根据n=$\frac{m}{M}$计算SO2、CO 物质的量之比,分子数目之比等于其物质的量之比,结合每个分子还愿意氧原子数目计算所含氧原子总数之比;
根据n=$\frac{m}{M}$计算SO2、CO 物质的量之比,同温同压下气体的体积之比等于其物质的量之比,同温同压下气体密度之比对相对分子质量之比.
解答 解:质量比为16:7的SO2、CO 分子的物质的量之比为$\frac{16}{64}$:$\frac{7}{28}$=1:1,则SO2、CO 分子的个数之比为 1:1,氧原子个数之比为1×2:1×1=2:1;
根据n=$\frac{m}{M}$可知,等质量的SO2、CO的物质的量之比为28g/mol:64g/mol=7:16,故同温同压下,等质量的SO2、CO体积比为7:16,同温同压下气体密度之比对相对分子质量之比,二者密度比为64:28=16:7,
故答案为:1:1;2:1;7:16;16:7.
点评 本题考查物质的量有关计算,难度不大,注意根据PV=nRT理解阿伏伽德罗定律及其推论.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素都属于纯净物 | B. | 金属氧化物都是碱性氧化物 | ||
| C. | 食醋、纯碱、食盐分别属于酸、碱、盐 | D. | 酸性氧化物不一定与水反应生成酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 水泥、玻璃、青花瓷、水晶、玛瑙、分子筛都属于硅酸盐工业产品 | |
| C. | 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理 | |
| D. | 通入过量的空气,可以使燃料充分燃烧,同时提高热量的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入甲烷的一极为正极 | |
| B. | 通入氧气的一极发生氧化反应 | |
| C. | 标准状况下,通入3.36L的CH4,则转移0.8mol的电子 | |
| D. | 该电池在工作时,溶液中的阳离子向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纯水的导电性很差,所以水不是电解质 | |
| B. | Na2O液态时能导电,所以Na2O是电解质 | |
| C. | 液态的铜导电性很好,所以铜是电解质 | |
| D. | 溶于水或熔融状态下能导电的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
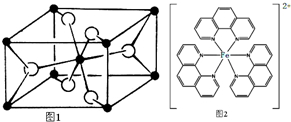
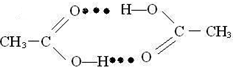 .
.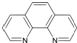 ),它能与Fe2+形成红色配合物(如右图2),
),它能与Fe2+形成红色配合物(如右图2),查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com