
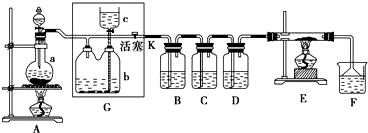
分析 (1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水;
(2)检验G的气密性需采取液压差法检验;
(3)G中b瓶是用来贮存Cl2的,则应选用一种Cl2在其中溶解度非常小的液体,一般选用饱和食盐水;
实验开始后,Cl2可与B中的氢硫酸反应得到浅黄色单质S沉淀,Cl2从C中置换出单质碘从而使C中溶液变蓝色;氯气与水反应生成盐酸和次氯酸,盐酸具有酸性,次氯酸具有漂白性基础解答;
(4)依据题意可知氯气与碳、水蒸气反应生成二氧化碳和氯化氢,依据原子个数守恒、得失电子守恒书写方程式;
解答 解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,化学方程式:MnO2+4HCl (浓) $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl (浓) $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O;
(2)检查装置G的气密性:关闭A中分液漏斗活塞G中活塞K(或用止水夹夹住A、G间的橡皮管并关闭G中活塞K),从c向容器内加水,c的下端浸入页面且c中液面高于b瓶内液面,若一段时间后c中液面不下降(或液面差保持不变),则说明气密性好;
故答案为;关闭A中分液漏斗活塞G中活塞K(或用止水夹夹住A、G间的橡皮管并关闭G中活塞K),从c向容器内加水,c的下端浸入页面且c中液面高于b瓶内液面,若一段时间后c中液面不下降(或液面差保持不变),则说明气密性好;
(3)G中b瓶是用来贮存Cl2的,则应选用一种Cl2在其中溶解度非常小的液体,一般选用饱和食盐水;
Cl2可与B中的氢硫酸反应得到浅黄色单质S沉淀,Cl2从C中置换出单质碘从而使C中溶液变蓝色,氯气与水反应生成盐酸和次氯酸,盐酸具有酸性,次氯酸具有漂白性,所以F中的现象:紫色石蕊溶液的颜色由紫色变为红色,再变为无色;
故答案为:饱和食盐水;上部空间由无色变黄绿色,溶液中有浅黄色沉淀生成;上部空间由无色变为黄绿色,溶液变蓝色;紫色石蕊溶液的颜色由紫色变为红色,再变为无色;
(4)依据题意可知氯气与碳、水蒸气反应生成二氧化碳和氯化氢,依据原子个数守恒、得失电子守恒,反应的化学方程式:2Cl2+C+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4HCl;
故答案为:2Cl2+C+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4HCl;
点评 本题综合考查了氯气的制法、性质、化学实验操作及实验装置等问题,把握氯气的性质以及相关实验操作方法是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+<Mg2+<Al3+<O2- | B. | S2->Cl->Na+>Al3+ | ||
| C. | Na<Mg<Al<S | D. | Cs<Rb<K<Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取碳酸钠晶体66g | |
| B. | 定容时,俯视观察刻度线 | |
| C. | 移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 | |
| D. | 定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选 项 | A | B | C | D |
| 物 质 | Na2O2 | H2O | HCl | NaCl |
| 所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键 |
| 所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 离子化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作及现象 | 结论 | |
| A | 将铜粉加入1.0mol•L-1Fe2(SO4)3溶液中,溶液变蓝 | 金属铁比铜活泼 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色. | Br-还原性强于Cl- |
| D | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结. | NH4Cl固体可以升华 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na、K元素的金属性依次减弱 | |
| B. | P、S、Cl元素的最高正价依次降低 | |
| C. | Li、Be、B的原子最外层电子数依次减少 | |
| D. | Na+、Mg2+、Al3+的离子半径依次减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
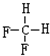 和
和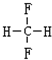
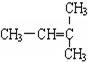 和CH2=CH-CH3
和CH2=CH-CH3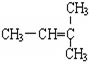 和
和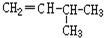
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
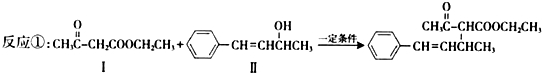
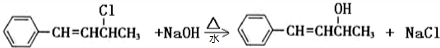 .
.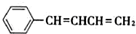 .
.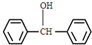 与
与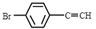 ,也可以发生类似反应①的反应,有机产物的结构简式为
,也可以发生类似反应①的反应,有机产物的结构简式为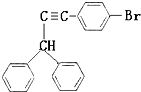 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com