
【题目】关于图中各装置的叙述不正确的是

A.装置①中X若为四氯化碳,可用于吸收氨气,并防止倒吸
B.装置②可检验溴乙烷发生消去反应得到的气体中含有乙烯
C.装置③的两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不相同
D.装置④能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀
科目:高中化学 来源: 题型:
【题目】某传感器工作原理如图所示。利用该传感器可以测定空气中NO、CO、NH3、SO2等有害气体的含量。下列说法正确的是

A. 传感器工作中,电子由Pt(Ⅰ)极经电流仪传到Pt(Ⅱ)极
B. 若M为熔融KOH,X为NH3,Y为N2,则负极的电极反应式为2NH3-6e- = N2+6H+
C. 若M是含O2-的固体电解质,X为NO,则正极的电极反应式为O2 + 4e- = 2O2-
D. 若X为CO,M为KOH溶液,则电池总反应为2CO+O2 = 2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]() 。在
。在![]() 的密闭容器中进行模拟合成实验,将
的密闭容器中进行模拟合成实验,将![]() 和
和![]() 通入容器中,分别在
通入容器中,分别在![]() 和
和![]() 反应,每隔一段时间测得容器中的甲醇的浓度如下:
反应,每隔一段时间测得容器中的甲醇的浓度如下:
| 10 | 20 | 30 | 40 | 50 | 60 |
300 | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500 | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
下列说法正确的是 ![]()
![]()
A.![]() 时,开始
时,开始![]() 内
内![]() 的平均反应速率
的平均反应速率![]()
B.反应达到平衡时,两温度下CO和![]() 的转化率之比均为
的转化率之比均为![]()
C.![]() 反应达到平衡时,放出的热量为
反应达到平衡时,放出的热量为![]()
D.![]() 时,若容器的容积压缩到原来的
时,若容器的容积压缩到原来的![]() ,则
,则![]() 增大,
增大,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】举世闻名的侯氏制碱法的工艺流程如下图所示,下列说法正确的是( )

A.往母液中加入食盐的主要目的是使![]() 更多的析出
更多的析出
B.从母液中经过循环Ⅰ进入沉淀池的主要是![]() 、
、![]() 和氨水
和氨水
C.沉淀池中反应的化学方程式:![]()
D.设计循环Ⅱ的目的是使原料氯化钠的利用率大大提升
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用自然界存在的角膜硼镁矿![]() 主要成分为
主要成分为![]() 制取金属镁和粗硼,工艺过程如下:
制取金属镁和粗硼,工艺过程如下:

根据以上信息回答下列问题:
(1)硼砂中硼的化合价 ______ ,溶于热水后,若需要调节pH为![]() 制取硼酸,写出该反应的离子方程式: ______ 。
制取硼酸,写出该反应的离子方程式: ______ 。
(2)从氯化镁晶体制得无水氯化镁的条件是 ______ ;其理由是 ______ ,若用惰性电磁电解![]() 溶液,写出电解过程的离子方程式: ______ 。
溶液,写出电解过程的离子方程式: ______ 。
(3)制得的粗硼可在一定条件与![]() 作用生产
作用生产![]() ,再提纯
,再提纯![]() ,
,![]() 沸点较低,提纯可采用 ______ ;高温时
沸点较低,提纯可采用 ______ ;高温时![]() 即可分解,得到高纯度硼。根据分解生成碘的量还可以测定粗硼的粗度。方法如下:
即可分解,得到高纯度硼。根据分解生成碘的量还可以测定粗硼的粗度。方法如下:
称取![]() 粗硼转化成纯
粗硼转化成纯![]() ,再完全分解,生成的碘用
,再完全分解,生成的碘用![]() 的
的![]() 溶液滴定至终点,消耗标准液
溶液滴定至终点,消耗标准液![]() 滴定原理:
滴定原理:![]()
①滴定终点判断应用 ______ 作指示剂;
②标准液应盛装在 ______ 滴定管中;
③该粗硼的纯度为 ______ 。
(4)![]() 酸性染料电池的反应机理为:
酸性染料电池的反应机理为:![]() ,则电池正极反应式为 ______ ;常温下,若起始电解液
,则电池正极反应式为 ______ ;常温下,若起始电解液![]() ,则电池工作一段时间后,电解液
,则电池工作一段时间后,电解液![]() ,此时溶液中
,此时溶液中![]() ______ ;当溶液
______ ;当溶液![]() 时,镁元素的主要存在形式是 ______ 。
时,镁元素的主要存在形式是 ______ 。![]() 已知:
已知:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
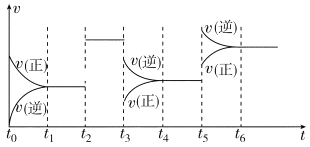
A.t2时加入了催化剂B.t3时降低了温度
C.t5时增大了压强D.t4~t5时间内X转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是

A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水液面回升时,正极反应式为:O2+2H2O+4e-===4OH-
D.U型管中溶液pH逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是

M | N | P | |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸 |
C | 银 | 锌 | 硝酸银溶液 |
D | 铜 | 铁 | 硝酸铁溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中正确的是( )
A.中和热的热化学方程式2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l);△H=-57.3 kJ/mol
B.氢气燃烧热的热化学方程式:H2(g)+![]() O2(g)=H2O(g);△H=-241.8 kJ/mol
O2(g)=H2O(g);△H=-241.8 kJ/mol
C.H218O2中加入H2SO4酸化的KMnO4:5H218O2+2MnO4-+6H+=518O2↑+2Mn2++8H2O
D.向CH2BrCOOH中加入足量的NaOH溶液并加热:CH2BrCOOH+OH-![]() CH2BrCOO-+H2O
CH2BrCOO-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com