
| A. | 高纯硅是工业上制造光导纤维的主要原料 | |
| B. | 开发和推广新能源汽车是实现低碳生活的途径之一 | |
| C. | 寻找高效催化剂,利用太阳能分解水是制取氢气的较理想方法 | |
| D. | 不需要通过化学反应就能从海水中获得淡水 |
分析 A.二氧化硅对光具有良好的全反射作用;
B.减少二氧化碳的排放为低碳生活方式;
C.寻找高效催化剂,利用太阳能分解水是制取氢气,节约能源;
D.从海水中获得淡水,利用蒸馏法.
解答 解:A.二氧化硅对光具有良好的全反射作用,则二氧化硅是工业上制造光导纤维的主要原料,故A错误;
B.减少二氧化碳的排放为低碳生活方式,则开发和推广新能源汽车是实现低碳生活的途径之一,故B正确;
C.寻找高效催化剂,利用太阳能分解水是制取氢气,节约能源,对环境无污染,是制取氢气的较理想方法,故C正确;
D.从海水中获得淡水,利用蒸馏法,则不需要通过化学反应,故D正确;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应为解答本题关键,侧重分析与应用能力的考查,注意化学与生活、环境的联系,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 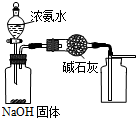 用图装置制取干燥纯净的NH3 | |
| B. | 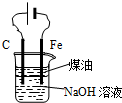 用图装置实验室制备Fe(OH)2 | |
| C. |  用图装置可以完成“喷泉”实验 | |
| D. |  用图装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子由Zn电极流出,经KOH溶液流向正极 | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: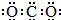 | |
| B. | 具有16个质子、16个中子和18个电子的微粒是${\;}_{16}^{32}$S | |
| C. | 甲酸钠的分子式:CHO2Na | |
| D. | 乙烯的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
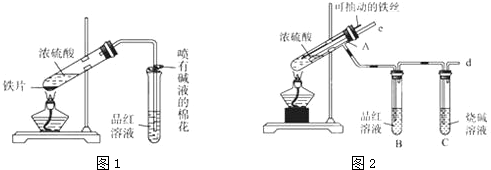
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑦ | B. | ③④⑤⑥⑦ | C. | ③⑥⑦ | D. | ②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com