
用NA表示阿伏伽德罗常数的数值,下列叙述正确的是( )
A.在同温同压下,相同体积的任何气体单质所含的分子数目一定相同
B.1L 0.5mol/L FeCl3溶液完全转化可得0.5NA个Fe(OH)3胶粒
C.标准状况下,22.4L苯含有的分子数为1NA
D.在常温常压下,11.2 L氮气所含的原子数目为NA
科目:高中化学 来源: 题型:实验题
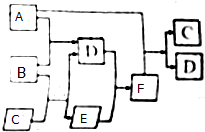 有A、B、C、D、E六种微粒,其中A-E五种微粒均由两元素组成且均含10个电子,它们有如图所示的转化关系:
有A、B、C、D、E六种微粒,其中A-E五种微粒均由两元素组成且均含10个电子,它们有如图所示的转化关系:查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上第一次月考化学卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列说法正确的是
A.标准状况下,22.4L盐酸含有NA个HCl分子
B.常温常压下,22.4LCO2和SO2混合气体含有2NA个O原子
C.常温常压下,8gCH4含有5NA个电子
D.1mol/LNaCl溶液中含有NA个Na+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高一上10月月考化学试卷(解析版) 题型:填空题
(1)有以下四种物质 ①22g二氧化碳;②5g氢气;③1.204╳1024个氮气分子; ④4℃时18g水,它们所含分子数最多的是 ; 质量最大的是 ;常温时体积最大的是 (填序号)。
质量最大的是 ;常温时体积最大的是 (填序号)。
(2)已知反应
①SO3+H20=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④2Na+2H2O=4NaOH +H2↑
+H2↑
⑤SiO2+2NaOH=Na2SiO3+H2O
上述反应中不属于氧化还原反应的是 (填序号,下同);属于氧化还原反应,其中H2O被氧化的是____ _ ;H2O被还原的是_ ;属于氧化还原反应,但H2O既不被氧化,也不被还原的是 。
(3)现有下列十种物质:
①蔗糖 ②熔融NaCl ③盐酸 ④铜丝 ⑤NaOH固体 ⑥SO2 ⑦CuSO4固体 ⑧K2O固体 ⑨液态H2SO4⑩液氯
上述物质中可导电的是 (填序号,下同);上述物质中不能导电,但属于电解质的是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高一上10月月考化学试卷(解析版) 题型:选择题
关于胶体的性质与应用,相关说法错误的是( )
A.静电除尘器除去空气中的飘尘是利用胶体粒子的带电性而加以除去
B.溶液和胶体均为呈电中性的分散系
C.FeCl3溶 液和Fe(OH)3胶体的本质区别是后者可以产生丁达尔现象
液和Fe(OH)3胶体的本质区别是后者可以产生丁达尔现象
D.由于胶粒之间的排斥作用,胶粒不易聚集成大的颗粒,所以胶体比较稳定
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:填空题
原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36, Y基态原子最外层电子数是其内层电子总数的3倍,X、W基态原子是同周期元素中未成对电子数最多的原子,X与Z的原子核内质子数之和等于W原子核内质子数,Z基态原子只有1个未成对的电子。
回答下列问题:
(1)已知化合物XZ3与H2Y(Y的氢化物)发生反应的化学方程式为XZ3+H2Y→XH3+HZY,则元素的电负性:Y Z(填“大于”或“小于”),化合物HZY分子的空间构型为 。
(2)X的一种氢化物的相对分子质量为32,1mol该氢化物中的σ键数是 ,该氢化物在水中的溶解性如何?主要原因是什么?
(3)元素Y 3个原子形成的单质分子与元素X、Y形成的一种离子互为等电子体,这种离子的化学式是 。
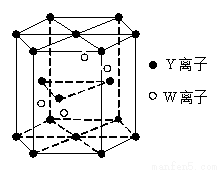
(4)基态W原子的电子排布式是 ,元素Y和W的一种化合物的晶体结构如右图所示,该晶体的化学式为 。(W处于晶体内部,Y分别处于晶胞面心、顶点、和内部)
(5)金属原子 (选填“钾”、“镁”、“铜”)形成的晶体的堆积方式,与上述晶胞中Y离子的堆积方式相同。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:选择题
有Fe2++H++NO3-→Fe3++NH4++H2O这样一个变化过程,下列叙述不正确的是
A.氧化剂和还原剂的物质的量之比为1:8
B.该过程说明Fe(NO3)2溶液不宜加酸酸化
C.每1 mol NO3-发生氧化反应,转移8 mol 电子
D.若把该反应设计为原电池,则负极反应为Fe2+-e- = Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
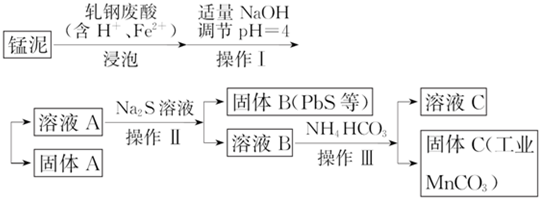
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com