
| A、Na2O+H2O═2NaOH | ||||
| B、2F2+2H2O═4HF+O2 | ||||
| C、Cl2+H2O═HCl+HClO | ||||
D、2H2O
|
| ||


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
 如图为配制250mL 0.2mol/L Na2CO3溶液的示意图.
如图为配制250mL 0.2mol/L Na2CO3溶液的示意图.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1升的0.1mol L-lNaHCO3溶液中含有0.1NA个HCO3- |
| B、17g氨气中含有的氢原子数为3NA |
| C、标准状况下,2.24LCCl4中含共价键数为0.4NA |
| D、常温常压下,2.24L甲烷中含有甲烷分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编组 | 强电解质 | 弱电解质 | 非电解质 |
| A | NaCl | HF | Cl2 |
| B | H2SO4 | BaCO3 | CO2 |
| C | AgCl | HClO | Cu |
| D | Ba(OH)2 | H2S | 蔗糖 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
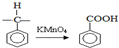
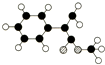 化学-选修有机化学基础
化学-选修有机化学基础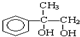 拟从
拟从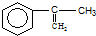 出发合成A.
出发合成A.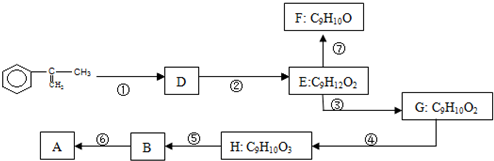
| HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Fe(NO3)2溶液中滴加稀硫酸 |
| B、将盐酸滴入NaAlO2溶液中 |
| C、向碳酸氢钠溶液中滴加氢氧化钠溶液 |
| D、加热溶有SO2的品红溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3+5 | -2+6 | -1+7 | +2 | +1+2 |
| 原子半径 | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |

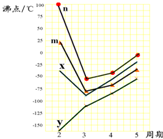
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com