
【题目】在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达到平衡,此时容器中气体的平均分子量为58。请计算(写出计算过程):
(1)10min内SO2的转化率;
(2)容器内反应前与平衡时的压强之比(最简整数比) ;
(3)该温度下的平衡常数。
【答案】60%;19/16;7.5L/mol
2SO2 + O2 == 2SO3
起始: 5 4.5 0
反应: 2X X 2X
平衡: 5-2X 4.5-X 2X
所以总物质的量为:5-2X+4.5-X+2X=9.5-X;由质量守恒定律,质量不变,为5×64+4.5×32=464g,所以![]() ,X=1.5mol。
,X=1.5mol。
(1)所以二氧化硫转化率为:2×1.5/5=60%
(2)恒容下压强比等于物质的量的比,(5+4.5):(9.5-1.5)=9.5:8=19:16
(3)达平衡时物质的量为:2mol,3mol,3mol;所以浓度为0.2mol/L,0.3mol/L,0.3mol/L,所以K=![]()
【解析】
2SO2 + O2 == 2SO3
起始: 5 4.5 0
反应: 2X X 2X
平衡: 5-2X 4.5-X 2X
所以总物质的量为:5-2X+4.5-X+2X=9.5-X;由质量守恒定律,质量不变,为5×64+4.5×32=464g,所以![]() ,X=1.5mol。
,X=1.5mol。
(1)所以二氧化硫转化率为:2×1.5/5=60%
(2)恒容下压强比等于物质的量的比,(5+4.5):(9.5-1.5)=9.5:8=19:16
(3)达平衡时物质的量为:2mol,3mol,3mol;所以浓度为0.2mol/L,0.3mol/L,0.3mol/L,所以K=![]()


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭体系中,可逆反应:A(s)+2B(g)![]() 2C(g) ΔH<0,不能作为该反应达到化学平衡的标志的是
2C(g) ΔH<0,不能作为该反应达到化学平衡的标志的是
①v正(B)=v逆(C) ②n(B)∶n(C)=1∶1 ③容器内压强不再改变
④容器内气体的密度不再改变 ⑤容器内混合气体的平均相对分子质量不再改变
A. ②③④⑤ B. ①③④ C. ②③ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列实验装置图,按要求作答:
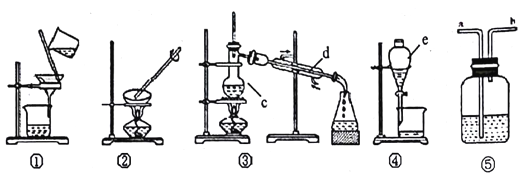
(1)装置中c、d、e的名称分别为_________
(2)分离下列物质,需要在哪套装置中进行?
I.干燥H2,可采用______(填装置序号)装置
II.除去食盐溶液中的水,可采用_____(填装置序号)装置
III. 淡化食盐水,可采用___(填装貿序号)装置
IV.实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可采用____(填装置序号)装置除去Ca(OH)2溶液中悬浮的CaCO3微粒
V.分离碘水中的碘应先选择装置_____(填装置序号),进行______和____操作,再用装置____(填装置序号)进行______操作。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某同学对相应反应的离子方程式所作的评价,其中对应的评价合理的是( )
编号 | 化学反应 | 离子方程式 | 评价 |
A | 把MgSO4溶液滴入Ba(OH)2溶液 | Mg2++2OH-=Mg(OH)2↓ | 正确 |
B | 氧化铜与稀盐酸反应 | CuO+2H+=Cu2++H2O | 错误,不反应 |
C | 向FeCl2溶液中通入氯气 | Fe2++Cl2=Fe3++2Cl- | 错误,电荷不守恒 |
D | 向沸水滴入饱和氯化 铁溶液 | Fe3++3H2O | 正确 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____,基态Fe2+中,核外电子占据最高能层的符号是____,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______,SCN—的几何构型为______,中心原子的杂化类型为_______。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________(填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列叙述正确的是( )
为阿伏加德罗常数的值。下列叙述正确的是( )
A.![]() 乙烷分子中含有的共价键数目为
乙烷分子中含有的共价键数目为![]()
B.![]() 完全溶于水转移的电子数为
完全溶于水转移的电子数为![]()
C.标准状况下,![]() 含有的原子数为
含有的原子数为![]()
D.![]() 乙烯和丙烯的混合物中含有的质子数为
乙烯和丙烯的混合物中含有的质子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
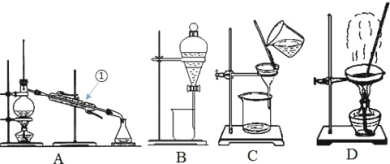
(1)从氯化钾溶液中得到氯化钾固体,选择装置____(填代表装置图的字母);
(2)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,可选择装置A,该分离方法的名称为_____,装置A中①的名称是______。
(3)实验室用B装置从碘水中分离出I2,将碘水和苯注入分液漏斗中充分振荡并静置后,碘主要溶解在_____(填“上层”或“下层”)液体中,该层溶液颜色为_____,该装置在分液时为使液体顺利下滴,应进行的具体操作_____。
Ⅱ.用胆矾晶体(CuSO4·5H2O)配制0.40mol/L的CuSO4溶液240mL,回答下列问题:
(1)所需仪器为:托盘天平、药匙、烧杯、量筒、玻璃棒、胶头滴管,还需要哪些玻璃仪器才能完成该实验,请写出:_____。
(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾_____g ③溶解 ④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀
(3)如图是该同学转移溶液的示意图,图中的错误是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜片与浓硫酸反应后,铜片表面变黑,为研究该黑色物质的成分,某化学兴趣小组查阅资料得知:该黑色物质可能含CuO、CuS、Cu2S及有可能被黑色掩盖颜色的Cu2O(砖红色)。该兴趣小组通过图1所示实验流程对该黑色物质的成分进行探究,其中步骤![]() 在图2装置中进行。
在图2装置中进行。
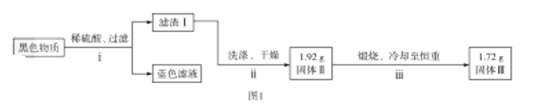
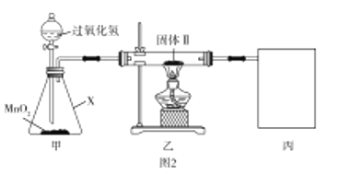
已知:Cu2O在酸中不稳定,生成Cu2+和Cu;铜的硫化物难溶于稀硫酸。回答下列问题:
(1)若测得滤渣Ⅰ中含Cu,写出“黑色物质”中加入稀硫酸发生反应生成Cu的离子方程式:__________。
(2)检验图2中整套装置气密性的方法是__________,仪器![]() 的名称是__________。
的名称是__________。
(3)步骤![]() 中检验固体Ⅱ洗涤干净的方法是__________。
中检验固体Ⅱ洗涤干净的方法是__________。
(4)通过计算确定固体Ⅱ中一定存在的硫化物是__________(写化学式)。
(5)为防止环境污染,丙装置可选用下列装置中的__________(填标号)
a.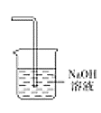 b.
b. c.
c.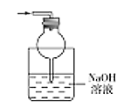 d.
d.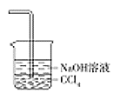
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 干冰升华和液氯气化时,都只需克服分子间作用力
B. 硫酸氢钠晶体溶于水,需要克服离子键和共价键
C. ![]() 和
和![]() 中,每个原子的最外层都具有8电子稳定结构
中,每个原子的最外层都具有8电子稳定结构
D. 石墨转化为金刚石时,既有共价键的断裂,又有共价键的形成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com