
(16分)
“白铁皮”即镀锌铁皮,镀锌层犹如铁皮的保护层,具有较强的耐腐蚀性,这层膜的厚度是判断白铁皮质量的重要指标,某研究性学习小组为了测定镀膜厚度,设计了下面的实验方案。
已知:
锌与强碱溶液反应的离子方程式为 :Zn+20H-=Zn022-+H2↑
锌的密度为dg/cm3
某学习小组同学设计了下图装置,使单侧面积为Scm2、质量为mg,的镀锌铁皮完全浸人6mol·L-1NaOH溶液中,充分反应。
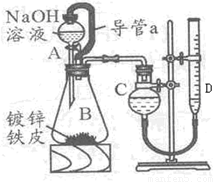
回答下列问题 :
(1)仪器名称A _B
(2)装置中导管 a 的作用是_________________________,
(3)干燥管C与量气管D (具有刻度的细长玻璃管)在反应前后液面高度有何要求:
反应前_______________,反应后 ,(答:“C中液面高于D中液面”,“C中液面低于D中液面”,“C中液面与D中液面相平”)其目的是_______________________。
(4)除了锌之外,另一种常见金属与强碱溶液反应的离子方程式为 。
(5)请设计实验证明,铁并未与强碱溶液反应而进入溶液 。
(6)实验前后量气管中液面读数分别为 V1mL、V2mL,(实验条件的气体摩尔体积为Vm L·mol-1), 则镀锌铁皮的厚度为h=_______________________cm(写出数学表达式)。
(7)请另设计一种测镀锌膜的厚度的方案,并用简单的方式表述出来:
|

(1)分液漏斗,锥形瓶
(2)将AB连通,平衡两者气压,使液体能顺利流下
(3)C中液面与D中液面相平;C中液面与D中液面相平;保证BC装置内的气压始终恒定。
(4)2Al + 2OH— + 2H2O = 2AlO2— + 3H2↑
(5)参考方案:取B 反应后剩余液,加入足量稀硝酸酸化,再滴入KSCN溶液,未见变红(其他方案合理亦可)
(6) h=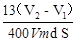
(7) 参考1:镀锌铁皮与强碱反应后,测剩余铁的质量,获得锌的质量,再进行换算
参考2:镀锌铁皮与盐酸反应后,根据金属的质量及产生氢气的体积进行换算
参考3:镀锌铁皮与盐酸反应后,在余下液体中加入足量强碱,过滤洗涤灼烧根据产生的氧化铁质量换算
(其他方案:在中学生所知范围内,合理即可)
【解析】
试题分析:(1)在做制备氯气的实验中用过这些一起,A为分液漏斗。B为锥形瓶。(2)为了使反应顺利进行,反应漏斗的试剂顺利滴下,需要保持压强的内外一致,因此需要导管a这个装置,装置中导管 a 的作用是:将AB连通,平衡两者气压,使液体能顺利流下。(3)本实验的关键是测量气体的体积。根据此装置的原理,应两次记录C中的读数,取其差值就是所得气体的体积,因此干燥管C与量气管D(具有刻度的细长玻璃管)在反应前后液面高度都是相平的。(4)根据所学知识,铝可与强碱溶液反应,离子方程式为:2Al + 2OH— + 2H2O = 2AlO2—
+ 3H2↑。(5)利用铁离子(Fe3+)的特征反应,遇KSCN溶液变红来检验铁是否参与了反应,方案为:取B 反应后剩余液,加入足量稀硝酸酸化,再滴入KSCN溶液,未见变红(其他方案合理亦可)。(6)根据体积只差算出放出H2的体积,利用化学方程式:Zn+20H-=Zn022-+H2↑,计算出Zn的质量,再用m=ρV=ρSh,得出h=m/(ρS),带入数据,解得h=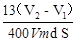 。(7)这题是开放题,只要符合题意的方案都是可以的。
。(7)这题是开放题,只要符合题意的方案都是可以的。
考点:化学实验 化学计算
点评:本题考查的是化学实验的基本操作及相关计算,测重基本实验操作能力考查。化学计算注重解题技巧,尤其是最后一题考查思维的深刻性和灵活性。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:2012-2013学年山东省平邑县曾子学校高二期中考试文科化学试卷(带解析) 题型:填空题
钢铁的生产和使用是人类文明和生活进步的一个重要标志。
(1)金属制品中的镀锡铁皮(马口铁)和镀锌铁皮(白铁皮)镀层部分破坏后,在潮湿的环境中, (填“马口铁”或“白铁皮”)更易锈蚀。
(2)人们常用氧化铁进行铝热反应来焊接钢轨,写出该铝热反应的化学方程式:
。
(3)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。
①铁锅所发生的腐蚀主要是 腐蚀。
②铁锅锈蚀的正极反应式为 。
(4)为防止轮船的船体在海水中腐蚀,一般在轮船身上装有一定数量的 (填“锌”或“铜”)块。
(5)工业炼铁原理的主要化学反应方程式(即赤铁矿生成铁)为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省丹东市宽甸二中高一上学期期末考试化学试卷(带解析) 题型:实验题
(16分)
“白铁皮”即镀锌铁皮,镀锌层犹如铁皮的保护层,具有较强的耐腐蚀性,这层膜的厚度是判断白铁皮质量的重要指标,某研究性学习小组为了测定镀膜厚度,设计了下面的实验方案。
已知:
锌与强碱溶液反应的离子方程式为 :Zn+20H-=Zn022-+H2↑
锌的密度为dg/cm3
某学习小组同学设计了下图装置,使单侧面积为Scm2、质量为mg,的镀锌铁皮完全浸人6mol·L-1NaOH溶液中,充分反应。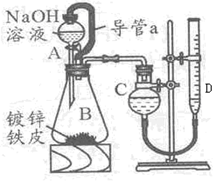
回答下列问题 :
(1)仪器名称A _B
(2)装置中导管 a 的作用是_________________________,
(3)干燥管C与量气管D (具有刻度的细长玻璃管)在反应前后液面高度有何要求:
反应前_______________,反应后 ,(答:“C中液面高于D中液面”,“C中液面低于D中液面”,“C中液面与D中液面相平”)其目的是_______________________。
(4)除了锌之外,另一种常见金属与强碱溶液反应的离子方程式为 。
(5)请设计实验证明,铁并未与强碱溶液反应而进入溶液 。
(6)实验前后量气管中液面读数分别为 V1mL、V2mL,(实验条件的气体摩尔体积为Vm L·mol-1), 则镀锌铁皮的厚度为h=_______________________cm(写出数学表达式)。
(7)请另设计一种测镀锌膜的厚度的方案,并用简单的方式表述出来:
|

查看答案和解析>>
科目:高中化学 来源:2014届山东省平邑县曾子学校高二期中考试文科化学试卷(解析版) 题型:填空题
钢铁的生产和使用是人类文明和生活进步的一个重要标志。
(1)金属制品中的镀锡铁皮(马口铁)和镀锌铁皮(白铁皮)镀层部分破坏后,在潮湿的环境中, (填“马口铁”或“白铁皮”)更易锈蚀。
(2)人们常用氧化铁进行铝热反应来焊接钢轨,写出该铝热反应的化学方程式:
。
(3)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。
①铁锅所发生的腐蚀主要是 腐蚀。
②铁锅锈蚀的正极反应式为 。
(4)为防止轮船的船体在海水中腐蚀,一般在轮船身上装有一定数量的 (填“锌”或“铜”)块。
(5)工业炼铁原理的主要化学反应方程式(即赤铁矿生成铁)为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com