
【题目】下列行为中符合安全要求的是
A. 进入煤矿井时,用火把照明
B. 节日期间,在开阔的广场燃放烟花爆竹
C. 用点燃的火柴在液化气钢瓶口检验是否漏气
D. 实验时,将水倒入浓硫酸配制稀硫酸
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:
【题目】随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
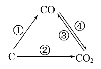
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可为;
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)===CO2(g)ΔH1<0;①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)===CO(g)+H2(g)ΔH2>0;②
再燃烧水煤气:2CO(g)+O2(g)===2CO2(g)ΔH3<0,③
2H2(g)+O2(g)===2H2O(g)ΔH4<0。④
则途径Ⅰ放出的热量________(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
(3)甲醇是一种可再生能源,具有开发和应用的广阔前景,已知反应2CH3OH(g)![]() CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
比较此时正、逆反应速率的大小:v正____v逆(填“>”“<”或“=”)。
(4)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
化学键 | N≡N | F—F | N—F |
键能/kJ·mol-1 | 941.7 | 154.8 | 283.0 |
则反应N2(g)+3F2(g)═2NF3(g)的ΔH=
(5)25℃、101kPa时,已知:
2H2O(g)═O2(g)+2H2(g)△H1
Cl2(g)+H2(g)═2HCl(g)△H2
2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是
A.△H3=△H1+2△H2B.△H3=△H1+△H2
C.△H3=△H1﹣2△H2D.△H3=△H1﹣△H2
(6)臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如6Ag(s)+O3(g)=3Ag2O(s)ΔH=-235.8kJ·mol-1,
已知:2Ag2O(s)=4Ag(s)+O2(g)ΔH=+62.2kJ·mol-1,
则O3转化为O2的热化学方程式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质) 制取绿矾(FeSO4·7H2O),某学习小组设计了如下流程:

下列说法错误的是
A. 酸浸时选用足量硫酸,试剂X为铁粉
B. 滤渣a主要含SiO2,滤渣b主要含Al(OH)3
C. 从滤液B得到绿矾产品的过程中,必须控制条件防止其氧化和分解
D. 试剂X若为过量NaOH溶液,得到的沉淀用硫酸溶解,再结晶分离也可得绿矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从薄荷中提取的薄荷醇可制成医药。薄荷醇的结构简式如下图,下列说法正确的是

A. 薄荷醇分子式为C10H20O,它是环己醇的同系物
B. 薄荷醇的分子中至少有12个原子处于同一平面上
C. 薄荷醇在Cu或Ag做催化剂、加热条件下能被O2氧化为醛
D. 在一定条件下,薄荷醇能发生取代反应、消去反应和聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列短周期元素性质的数据:下列关于表中11种元素的说法正确的是
元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
原子半径 (10-10m) | - | 0.37 | 0.74 | 0.75 | 0.77 | 0.82 | 0.99 | 1.10 | 1.52 | 1.60 | 1.86 |
最高或最低化合价 | 0 | +1 | +5 | +4 | +3 | +7 | +5 | +1 | +2 | +1 | |
-2 | -3 | -4 | -1 | -3 |
A. 上表中11种元素中形成的非金属单质都有非极性共价键
B. ②⑨处于同一周期,④⑧处于同一主族
C. 上表中11种元素中最高价氧化物对应的水化物中⑦号酸性最强
D. ⑥原子结构示意图为: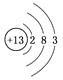
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
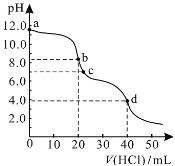
A. a点溶液呈碱性的原因用离子方程式表示为:CO![]() +2H2O
+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. c点处的溶液中c(Na+)-c(Cl-)=c(HCO![]() )+2c(CO
)+2c(CO![]() )
)
C. 滴定过程中使用甲基橙作为指示剂比酚酞更准确
D. d点处溶液中水电离出的c(H+)大于b点处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E三种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出元素的名称:C__________,D___________。
(2)写出元素的原子结构示意图:A______________,B______________,二者离子半径:_______>_________ (填化学式,下同)。
(3)A、B的最高价氧化物的水化物的碱性:______________>______________。
(4)D、E的气态氢化物的稳定性:______________>______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种物质中,①Ar,②CO2 , ③SiO2 , ④NaOH,⑤K2S,只存在共价键的是 , 只存在离子键的是 , 既存在离子键又存在共价键的是 , 不存在化学键的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质, A为是生产、生活中用量最大、用途最广的金属单质,室温下B是黄绿色气体,C为无色气体。在一定条件下相互转化的关系如图所示。
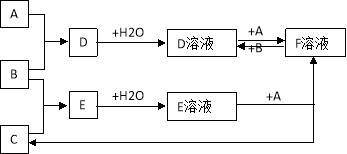
请回答以下问题:
(1)A、B、C分别是什么物质:A是 ,B是 ,C是,F是 (填化学式)
(2)写出A和B生成D的化学方程式: ,向D溶液中加
入 溶液可看到溶液变血红色。
(3)写出F溶液中加入B的离子方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com