
【题目】2013年12月2日,“嫦娥三号”探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察。“长征”系列火箭用偏二甲肼(C2H8N2)作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体。
(1)写出反应的化学方程式:_____________________________________________。
(2)该反应是________(填“放热”或“吸热”)反应,反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量,断开化学键________的总能量小于形成化学键________的总能量(填“吸收”或“放出”)。
(3)如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,这个规律称为盖斯定律。据此回答下列问题。
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。
已知:C3H8(g)―→CH4(g)+HC≡CH(g)+H2(g) ΔH1=+156.6 kJ·mol-1
CH3CH=CH2(g)―→CH4(g)+HC≡CH(g) ΔH2=+32.4 kJ·mol-1
则相同条件下,丙烷脱氢得丙烯的热化学方程式为________________________________。
(2)已知:Na2CO3·10H2O(s)===Na2CO3(s)+10H2O(g)ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________________。
【答案】 C2H8N2+2N2O4![]() 2CO2↑+3N2↑+4H2O 放热 大于 吸收 放出 C3H8(g)―→CH3CH=CH2(g)+H2(g) ΔH=+124.2 kJ/mol Na2CO3·H2O(s)===Na2CO3(s)+H2O(g) ΔH=+58.73 kJ/mol
2CO2↑+3N2↑+4H2O 放热 大于 吸收 放出 C3H8(g)―→CH3CH=CH2(g)+H2(g) ΔH=+124.2 kJ/mol Na2CO3·H2O(s)===Na2CO3(s)+H2O(g) ΔH=+58.73 kJ/mol
【解析】(1)偏二甲肼(C2H8N2)作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体,据此写出化学方程式;(2)该反应能提供飞船飞行所需的能量,据此分析反应吸放热和反应物的总能量、生成物的总能量之间的关系.(3)①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ·mol-1,②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJ·mol-1,依据盖斯定律①-②得到C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ·mol-1,据此进行分析;(2)同理由盖斯定律①-②,可得。
(1)偏二甲肼(C2H8N2)作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体,故化学方程式为:C2H8N2+2N2O4![]() 2CO2↑+3N2↑+4H2O ;(2)该反应能提供飞船飞行所需的能量,故此反应为放热反应,则反应物的总能量大于生成物的总能量,断开化学键所吸收的总能量小于形成化学键放出的总能量。(3)(1)①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ·mol-1,②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJ·mol-1,依据盖斯定律①-②得到C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ·mol-1。(2)①Na2CO3·10H2O(s)═Na2CO3(s)+10H2O(g)△H1=+532.36kJ·mol-1,②Na2CO3·10H2O(s)═Na2CO3·H2O(s)+9H2O(g)△H1=+473.63kJ·mol-1,由盖斯定律①-②得到:Na2CO3·H2O(s)═Na2CO3(s)+H2O(g)△H1=+58.73kJ·mol-1。
2CO2↑+3N2↑+4H2O ;(2)该反应能提供飞船飞行所需的能量,故此反应为放热反应,则反应物的总能量大于生成物的总能量,断开化学键所吸收的总能量小于形成化学键放出的总能量。(3)(1)①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ·mol-1,②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJ·mol-1,依据盖斯定律①-②得到C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ·mol-1。(2)①Na2CO3·10H2O(s)═Na2CO3(s)+10H2O(g)△H1=+532.36kJ·mol-1,②Na2CO3·10H2O(s)═Na2CO3·H2O(s)+9H2O(g)△H1=+473.63kJ·mol-1,由盖斯定律①-②得到:Na2CO3·H2O(s)═Na2CO3(s)+H2O(g)△H1=+58.73kJ·mol-1。


科目:高中化学 来源: 题型:
【题目】下列四种元素中,单质的氧化性最强的是( )
A.原子最外层电子数为次外层电子数的2倍
B.第三周期ШA族元素
C.原子核外L层电子数为K层电子数的3倍
D.第16号元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
t∕min | 2 | 4 | 7 | 9 |
n(Y)∕mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前4min的平均反应速率υ(Z)=0.0125molL-1min-1
B.其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,达平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是
A.K2CO3=K++CO32-B.NaOH=Na++O2-+H+
C.MgSO4=mg2++SO42-D.Ba(NO3) 2=Ba2++2NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素及其化合物的表示正确的是
A. 氮气的电子式:![]()
B. CH4分子的球棍模型: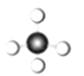
C. Mg2+结构示意图: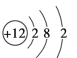
D. 质子数为92、中子数为146的U原子:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/mol
S(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(1)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式_______________________________。
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,发生上述(1)中回收硫的反应。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率ν(CO)= _________,该温度下反应化学平衡常数K=____________(L·mol-1)
(3)在不同条件下,向2L恒容密闭容器中通入2molCO和1molSO2,反应体系总压强随时间的变化如图(Ⅰ)所示:
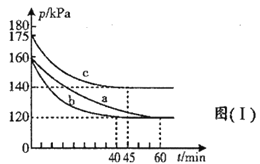
①图(Ⅰ)中三组实验从反应开始至达到平衡时,v(CO)最大的为___________(填序号)
②与实验a相比,c组改变的实验条件可能是_________________。
(4)“亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图(Ⅱ)所示,b点时溶液pH=7,则n(NH4+)∶n(HSO3-)=______。

(5)间接电化学法可除NO。其原理如图(Ⅲ)所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)_______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:

针对表中的①~⑩号元素,用元素符号或化学式填空:
(1)在这些元素中,最易得电子的元素是____,失电子能力最强的元素是________。
(2)化学性质最不活泼的元素是____,其原子结构示意图为________。
(3)④、⑨的最高价氧化物对应的水化物在溶液中反应的离子方程式是________。
(4)在①②③④四种元素,原子半径由大到小的顺序是________。
(5)元素⑥、⑦、⑩的最高价氧化物对应的水化物中,酸性最强的是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com