
| A�� | 0.1mol•L-1��ˮ�У�c��OH-��=c��NH4+�� | |
| B�� | 10 mL 0.02mol•L-1HCl��Һ��10 mL 0.02mol•L-1Ba��OH��2��Һ��ֻ�ϣ�����Ϻ���Һ�����Ϊ20 mL������Һ��pH=12 | |
| C�� | ��0.1mol•L-1CH3COONa��Һ�У�c��OH-��=c��CH3COOH��+c��H+�� | |
| D�� | 0.1mol•L-1ij��Ԫ����ǿ����NaHA��Һ�У�c��Na+��=2c��A2-��+c��HA-��+c��H2A�� |
���� A����ˮ����Ҫ�ɷ���NH3•H2O��NH3•H2O��һԪ����������NH4+��OH-��H2OҲ�����OH-��
B�������Ϻ��c��OH-�����ټ�����Һ��pH��
C���������غ��ϵʽ�������غ��ϵʽ���ɽ��
D������NaHA��ѧʽ����Һ��Na+Ũ�ȵ��ں�AԪ����Ũ�Ⱥͣ�
��� �⣺A����ˮ����Ҫ�ɷ���NH3•H2O��NH3•H2O��һԪ����������NH4+��OH-��H2OҲ�����OH-����c��NH4+����c��OH-������A����
B��10ml0.02mol/L��HCl��Һ��10ml0.02mol/L��Ba��OH��2��Һ��ֻ�Ϻ�����Ϻ���Һ���Ϊ20ml����Ӧ�����Һ��C��OH-��c��OH-��=$\frac{0.04mol/L��0.01L-0.02mol/L��0.01L}{0.02L}$=0.01 mol•L-1��c��H+��=$\frac{1��1{0}^{-14}}{0.01}$=10-12mol/L����pH����12����B��ȷ��
C����Һ�д��ڵ��������ǣ�H+��Na+���������ǣ�OH-��CH3COO-�����ݵ���غ��У���C��H+��+C��Na+��=C��OH-��+C��CH3COO-�������ݴ������̼Ԫ���غ㣩д�������غ��ϵ�ã�C��Na+��=C��CH3COO-��+C��CH3COOH���ڣ����ڴ���ٿɵã�c��OH-��=c��CH3COOH��+c��H+������C��ȷ��
D��AԪ�صĴ�����ʽΪ��A2-��HA-��H2A�����������غ㣬NaHA�У�c��Na+����c����A����=1��1��0.1mol•L-1ij��Ԫ����ǿ����NaHA��Һ�У�c��Na+��=c��A2-��+c��HA-��+c��H2A������D����
��ѡBC��
���� ���⿼����������ʵĵ��롢pH���㼰����ˮ���֪ʶ��Ҫ���ǵ����ˮ�⣬ע�������غ㡢ˮ���غ��Ӧ�ã���Ŀ�Ѷ��еȣ�


 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
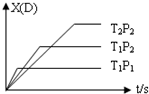 ��֪���淴Ӧ mA��g��+nB��g��?pC��g��+qD��g������Ӧ��D�����ʵ�������X��D����ʱ��t�Ĺ�ϵ��ͼ��������������ȷ���ǣ�������
��֪���淴Ӧ mA��g��+nB��g��?pC��g��+qD��g������Ӧ��D�����ʵ�������X��D����ʱ��t�Ĺ�ϵ��ͼ��������������ȷ���ǣ�������| A�� | ����ӦΪ���ȷ�Ӧ | B�� | m+n��p+q | ||
| C�� | T1��T2 | D�� | P1��P2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | þ���Ͻ�������mg | HCl���ʵ���/mol | ���������/mL |
| �� | 255 | X | 280 |
| �� | 385 | X | 336 |
| �� | 459 | X | 336 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �л��� | �������� | ������Һ | ����������ͭ | ������ |
| A | �����кͷ�Ӧ | ����Ӧ | �ܽ� | �ų����� |
| B | ����Ӧ | ����������Ӧ | ���ɺ�ɫ���� | �ų����� |
| C | ����ˮ�ⷴӦ | ����������Ӧ | ���ɺ�ɫ���� | ����Ӧ |
| D | ����ˮ�ⷴӦ | ����Ӧ | ����Ӧ | ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ı�ijһ������ʹv��������v���棩���ı䣬��ѧƽ��һ���ƶ� | |
| B�� | �ı�ijһ������ʹv�䣨������v�䣨�棩���䣬��ѧƽ��һ�������ƶ� | |
| C�� | �ı�ijһ������ʹv�䣨��������v�䣨�棩���䣬��ѧƽ��һ�������ƶ� | |
| D�� | �ı�ijһ������v�䣨������v�䣨�棩ͬʱ�����ͬʱ��Сʱ����ѧƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | +3 | B�� | +2 | C�� | -2 | D�� | +1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����Һ���еμ�KSCN��Һ����Һ��ɫ��죬��ԭ��ʯ��Ʒ�д���Fe3+ | |
| B�� | ����Һ���еμ���������������Һ��һ�����ֺ��ɫ���� | |
| C�� | ����Һ���еμ�KSCN��Һ����Һ��ɫ��죬��ԭ��ʯ��Ʒ�д���Fe3+ | |
| D�� | �ÿ�ʯһ��Ϊ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com