
【题目】在①CH4、②C2H2、③C2H4、④C2H6、⑤苯中
(1)能使酸性高锰酸钾溶液褪色的是__________。(填序号,下同)
(2)相同物质的量,在氧气中完全燃烧时消耗氧气最多的是________;
(3)相同质量,在氧气中完全燃烧时消耗氧气最多的是____,耗氧量、生成CO2和水都相等的是___________。
【答案】②③ ⑤ ① ②⑤
【解析】
(1)烷烃、苯不能使酸性高锰酸钾溶液褪色,烯烃、气体酸性高锰酸钾溶液褪色;
(2)物质化学式中含有的C、H原子数越多,完全燃烧消耗氧气的物质的量就越多;
(3)根据等质量的C、H完全燃烧消耗氧气的多少分析判断。
(1)①CH4是烷烃,与酸性高锰酸钾溶液不反应,因而不能使酸性高锰酸钾溶液褪色;②C2H2是炔烃,含有碳碳三键,可以被酸性高锰酸钾溶液氧化为使其褪色;
③C2H4是烯烃,含有碳碳双键,可以被酸性高锰酸钾溶液氧化为使其褪色;
④C2H6是烷烃,与酸性高锰酸钾溶液不反应,因而不能使酸性高锰酸钾溶液褪色;
⑤苯是芳香烃,无不饱和的碳碳双键,不能被酸性高锰酸钾溶液氧化,因而不能使其褪色,
故能够使酸性高锰酸钾溶液褪色是②③;
(2)假设这几种物质的物质的量都是1mol。①1molCH4完全燃烧消耗O2的物质的量是2mol;②1molC2H2完全燃烧消耗O2的物质的量是2.5mol;③1molC2H4完全燃烧消耗O2的物质的量是3mol;④1molC2H6完全燃烧消耗O2的物质的量是3.5mol;⑤1mol苯完全燃烧消耗O2的物质的量是7.5mol;可见相同物质的量,在氧气中完全燃烧时消耗氧气最多的是苯,合理选项是⑤;
(3)给出的物质都是烃,含有C、H两种元素,根据氢气、碳单质燃烧方程式:2H2+O2![]() 2H2O,C++O2
2H2O,C++O2![]() CO2可知:消耗1molO2,需要4gH,需要12gC,可见等质量的有机物中H元素的含量越多,完全燃烧消耗的氧气越多。在上述五种物质中CH4的H元素含量最高,因此相同质量,在氧气中完全燃烧时消耗氧气最多的是甲烷,合理选项是①;
CO2可知:消耗1molO2,需要4gH,需要12gC,可见等质量的有机物中H元素的含量越多,完全燃烧消耗的氧气越多。在上述五种物质中CH4的H元素含量最高,因此相同质量,在氧气中完全燃烧时消耗氧气最多的是甲烷,合理选项是①;
耗氧量、生成CO2和水都相等,说明物质的最简式相同,观察上述五种物质可知乙炔和苯最简式相同,因此等质量的这两种物质完全燃烧耗氧量、生成CO2和水都相等,合理选项是②⑤。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】实验室做乙醛和银氨溶液发生银镜反应的实验时:
(1)为产生光亮的银镜,试管应先用______溶液煮沸,倒掉煮沸液后再用清水将试管冲洗干净。
(2)配制银氨溶液时向盛有__________溶液的试管中逐滴滴加__________溶液边滴边振荡直到__________为止。有关化学反应的离子方程式为:①_____________________;②_________________________。
(3)加热时应用________加热,产生银镜的化学方程式:____________________。
(4)实验室配制银氨溶液时若向AgNO 3 溶液中加入氨水形成银氨溶液时,应防止加入氨水过量,否则容易生成容易爆炸的________,试剂本身也失去灵敏性。配制好的银氨溶液不可久置,否则会生成________,从溶液中析出这种沉淀,哪怕是用玻璃棒刮擦也会分解发生猛烈的爆炸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上消除氮氧化物的污染,可用如下反应:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol
在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法不正确的是
A. 10 min内,T1时v(CH4)T2时小 B. 温度:T1<T2
C. ΔH:a < 0 D. 平衡常数:K(T1)<K(T2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,试根据实验回答:
(1)将准确称量好的2.0 g烧碱样品配成100mL待测液,需要的主要玻璃仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有_______、________________。
(2)用碱式滴定管量取10.00mL待测液,置于锥形瓶中,同时滴加1-2滴指示剂。化学上常选用的指示剂有酚酞或____________。
(3)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视__________________,直到滴定到终点,若选择酚酞作为指示剂,判断滴定终点的标志是___________________________。
(4)根据下列数据,测得c(NaOH)=________。烧碱的纯度=____________。
滴定 次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
第三次 | 10.00 | 1.00 | 24.10 |
(5)以标准的盐酸溶液滴定未知浓度的氢氧化钠溶液,下列操作引起待测液浓度偏小的是 _______________(填序号)。
①读数:滴定前平视,滴定后俯视②未用待测液润洗碱式滴定管
③用待测液润洗锥形瓶④不小心将标准液滴在锥形瓶外面
⑤滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于SiO2的说法中错误的是
A.纯净的SiO2是光纤制品的基本原料
B.SiO2能与NaOH溶液反应生成盐
C.SiO2高温下能与CaO反应生成盐
D.SiO2能与氢氟酸反应,因此它属于碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
①C2H2(g)+![]() O2(g)
O2(g)![]() 2CO2(g)+H2O(l) ΔH1=-1 301.0 kJ·mol-1
2CO2(g)+H2O(l) ΔH1=-1 301.0 kJ·mol-1
②C(s)+O2(g)![]() CO2(g) ΔH2=-393.5 kJ·mol-1
CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH3=-285.8 kJ·mol-1
H2O(l) ΔH3=-285.8 kJ·mol-1
则反应④2C(s)+H2(g)![]() C2H2(g)的ΔH为( )
C2H2(g)的ΔH为( )
A. -228.2 kJ·mol-1B. +228.2 kJ·mol-1
C. +1301.0 kJ·mol-1D. +621.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
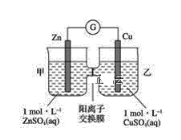
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,乙池溶液的总质量增加
C. 电池工作一段时间后,甲池的c(SO42-)减小
D. 阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有氯化钠和碘化钠的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为 17.55 g。
(1)原混合物中碘化钠的质量是________。
(2)原混合物中氯化钠的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离或除杂的方法正确的是
A.分离硬脂酸钠和甘油,加饱和食盐水盐析,过滤
B.除去乙酸乙酯中的乙酸,加烧碱溶液,蒸馏
C.分离苯酚和酒精混合液,分液
D.除去淀粉溶液中NaCl,过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com