
【题目】现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方案。
实验编号 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 25℃ | 三氧化二铁 | 10mL 5%H2O2 |
甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
甲、乙两小组得出如图数据:

关于该实验下列叙述不正确的是
A.  中,O2是氧化产物
中,O2是氧化产物
B. 甲小组实验得出的结论是Fe2O3比MnO2催化效率更高
C. 甲小组实验也可以测定25℃时,在相同时间内产生氧气的体积
D. 乙组研究的影响因素的数据分析,相同条件下H2O2在碱性环境下放出气体速率较快
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.0.1 L 1 mol/L K2SO4 溶液中含有氧原子数为0.4NA
B.67.2L氯气所含的原子数是6NA
C.常温常压下,11.2 LO2含有电子数为8NA
D.在标准状况下,2.24LN2和O2的混合气体所含原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
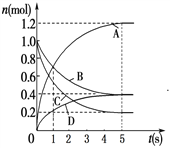
A. 该反应的化学方程式为6A+2 D![]() 3B+4C
3B+4C
B. 反应进行到1 s时,v(A)=v(B)
C. 反应进行到5 s时,B的平均反应速率为0.06mol/(L·s)
D. 反应进行到5 s时,v(A)=v(B)=v(C)=v(D)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C原子第一至第四电离能如下: I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·mol-1,I4=10540 kJ·mol-1 |
D原子核外所有p轨道全满或半满 |
E元素的主族序数与周期数的差为4 |
F是前四周期中电负性最小的元素 |
G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
![]() ,该同学所画的电子排布图违背了____________。
,该同学所画的电子排布图违背了____________。
(4)G位于第_____族_____区,该元素的核外电子排布式为_____________________________。
(5)检验F元素的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的分子结构如图所示。现有试剂:①Na ②H2/Ni ③Ag(NH3)2OH ④新制Cu(OH)2 ⑤NaOH ⑥酸性KMnO4溶液。能与该化合物中两个或两个以上官能团都发生反应的试剂有( )
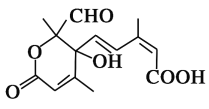
A.①②⑤⑥ B.①②④⑥ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随加水体积变化的曲线如图所示。下列说法正确的是

A. HB的酸性强于HA
B. a点溶液的导电性大于b点溶液
C. 同浓度的NaA与NaB溶液中,c(A-)=c(B-)
D. 加水稀释到pH相同时,酸HA、HB用到的水V(A)小于V(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol/L氨水分别滴定20.0mL 0.1mol/L的盐酸和醋酸,曲线如图所示,下列叙述中不正确的是

A. x=20
B. Ⅰ曲线表示的是滴定醋酸的曲线
C. 滴定过程中![]() 的值逐渐减小
的值逐渐减小
D. 当Ⅰ曲线和Ⅱ曲线pH均为7时,某一溶液中的c(Cl-)大于另一溶液中的c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家倡导推进传统产业改造升级,引导企业创新优化产业结构。其根本目的是节能减排,“减排”的关键是减少CO2排放,而“减排”的重要手段是合理利用CO2。回答下列问题:
(1)CO2的电子式是___。
(2)利用CO2可合成尿素[CO(NH2)2],合成原料除CO2外,还有NH3。该方法制备尿素的化学方程式是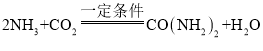 ,该方法制备尿素一般需
,该方法制备尿素一般需![]() >2,即NH3过量,原因是____。
>2,即NH3过量,原因是____。
(3)利用太阳能,以CO2为原料制取炭黑的流程如图1所示:一定条件“过程1”生成1mol炭黑的反应热为ΔH1;“过程2”的热化学方程式为:2Fe3O4(s)![]() 6FeO(s)+O2(g) ΔH2。则图1中制备炭黑的热化学方程式为___。
6FeO(s)+O2(g) ΔH2。则图1中制备炭黑的热化学方程式为___。

(4)将1mol CO2和3mol H2充入容积为1L的恒容密闭容器中,发生反应:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。
C2H4(g)+4H2O(g) ΔH。
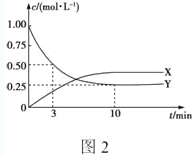
①图2是测得的该反应中X、Y的浓度随时间变化的曲线,其中X为___(写化学式),反应达到平衡时的平均反应速率v(H2)=____mol·L-1·min-1。
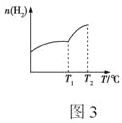
②不同温度下平衡时,混合气体中H2的物质的量随温度的变化曲线如图3所示,则该反应的ΔH____0(填“>”“<”或“不能确定”);测定温度小于T2时,反应体系中无O2存在,则T1~T2的温度范围内,H2的物质的量急剧增大的原因可能是____。
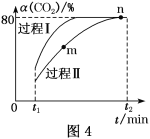
(5)CO2还可以合成甲醇:CO2(g)+3H2(g)![]() H2O(g)+CH3OH(g) ΔH=-53.7 kJ·mol-1,一定条件下,将1 mol CO2和2.8 mol H2充入容积为2L的绝热密闭容器中,发生上述反应。CO2的转化率[α(CO2)]在不同催化剂作用下随时间的变化曲线如图4所示。n点的平衡常数K=___。
H2O(g)+CH3OH(g) ΔH=-53.7 kJ·mol-1,一定条件下,将1 mol CO2和2.8 mol H2充入容积为2L的绝热密闭容器中,发生上述反应。CO2的转化率[α(CO2)]在不同催化剂作用下随时间的变化曲线如图4所示。n点的平衡常数K=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列有机物的系统命名或结构简式:

(1)_____________
(2)_____________
(3)4,4,5-三甲基-2-己炔 _______________
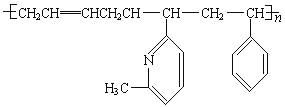
(4)新型弹性材料“丁苯吡橡胶”的结构简式如下:其单体为______________(有几种写几种)
(5)如下表所示,为提纯下列物质(括号内为少量杂质),填写所选用的除杂试剂与主要分离方法
不纯物质 | 除杂试剂 | 分离方法 | |
1 | 溴苯(Br2) | __________ | __________ |
2 | 乙醛(乙酸) | __________ | __________ |
3 | 乙酸乙酯(乙酸) | __________ | __________ |
4 | 乙醇(苯酚) | __________ | __________ |
5 | 硝基苯(硝酸) | __________ | __________ |
(6)①C5H12O的醇,在一定条件下能发生催化氧化反应,产物能与新制的氢氧化铜反应生成红色沉淀,醇的核磁共振氢谱中有三组峰,写出满足上述条件的醇的结构简式______
②C5H12O的醇,在一定条件下不能发生消去反应,写出满足条件的醇的结构简式______
③分子式为C5H12O,不能与金属钠反应.核磁共振氢谱中有四组峰,峰的面积比为3:2:1:6,写出满足上述条件的物质的结构简式______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com