
分析 (1)元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素;
(2)Fe是26号元素,其原子核外有26个电子,3d、4s电子为其价电子,根据构造原理书写其核外电子排布式;原子个数相等、价电子数相等的微粒为等电子体;
(3)CaO和NaCl晶胞结构类型相同,则每个Ca2+周围与它最近且等距的Ca2+个数=3×8÷2;离子晶体晶格能与离子电荷成正比、与离子半径成反比.
解答 解:(1)元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以第一电离能N>O,故答案为:>;
(2)Fe是26号元素,其原子核外有26个电子,3d、4s电子为其价电子,根据构造原理书写Fe核外电子排布式为3d64s2;原子个数相等、价电子数相等的微粒为等电子体,与CO等电子体的微粒有N2、CN-、C22-等;
故答案为:3d64s2;N2、CN-、C22-等;
(3)CaO和NaCl晶胞结构类型相同,则每个Ca2+周围与它最近且等距的Ca2+个数=3×8÷2=12;离子晶体晶格能与离子电荷成正比、与离子半径成反比,CaO中离子电荷大于NaCl,所以晶格能CaO大于NaCl,
故答案为:12;大于.
点评 本题考查物质结构和性质,涉及晶胞计算、晶格能、原子核外电子排布、第一电离能等知识点,综合性较强,难点是配位数的计算,注意第一电离能的规律和异常现象,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O+CO32- | |
| B. | 漂白粉溶液中通入过量CO2气体:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | |
| C. | 向NH4Al(SO4)2溶液中逐渐滴入加入Ba(OH)2溶液恰好使SO42-反应完全: 2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O | |
| D. | FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、CH3COOH、CO32-、NO3- | B. | Fe3+、Na+、SCN-、Cl- | ||
| C. | Ba2+、Na+、OH-、HCO3- | D. | H+、K+、Fe3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
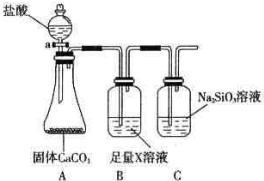
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1摩尔H2O所含质子数为12NA | |
| B. | 2克氢气所含原子数为NA | |
| C. | 0.5摩尔单质铝与足量盐酸反应转移电子数为1.5NA | |
| D. | 标准状况下,1升水所含分子数为$\frac{1}{22.4}$ NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
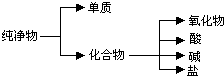 (1)纯净物根据其组成和性质可进行如图分类:如图所示的分类方法属于B(填序号)
(1)纯净物根据其组成和性质可进行如图分类:如图所示的分类方法属于B(填序号)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
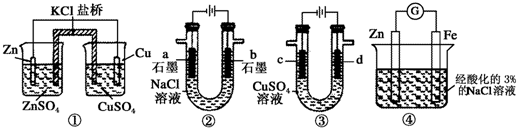
| A. | 装置①中,一段时间后SO42-浓度增大 | |
| B. | 装置②中滴入酚酞,a极附近变红 | |
| C. | 用装置③精炼铜时,c极为粗铜 | |
| D. | 装置④中发生吸氧腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com