
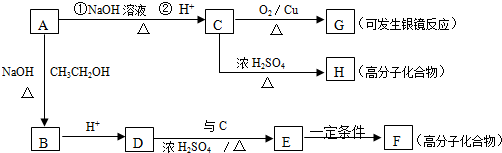
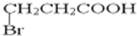 ��A����������ˮ��Һ����ʱ����ȡ����Ӧ��Ȼ���ữ����C��C�Ľṹ��ʽΪHOCH2CH2COOH��C����������Ӧ����G��G�Ľṹ��ʽΪOHCCH2COOH��C����������Ӧ���ɸ߷��ӻ�����H����ṹ��ʽΪ
��A����������ˮ��Һ����ʱ����ȡ����Ӧ��Ȼ���ữ����C��C�Ľṹ��ʽΪHOCH2CH2COOH��C����������Ӧ����G��G�Ľṹ��ʽΪOHCCH2COOH��C����������Ӧ���ɸ߷��ӻ�����H����ṹ��ʽΪ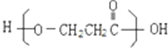 ��A��NaOH����Һ����ʱ��A������ȥ��Ӧ����B��B�Ľṹ��ʽΪCH2=CHCOONa��BȻ���ữ����D����D�Ľṹ��ʽΪCH2=CHCOOH��D��C��Ũ���������������������·�Ӧ����E��E�Ľṹ��ʽΪCH2=CHCOOCH2CH2COOH��E�����Ӿ۷�Ӧ����F��F�Ľṹ��ʽΪ
��A��NaOH����Һ����ʱ��A������ȥ��Ӧ����B��B�Ľṹ��ʽΪCH2=CHCOONa��BȻ���ữ����D����D�Ľṹ��ʽΪCH2=CHCOOH��D��C��Ũ���������������������·�Ӧ����E��E�Ľṹ��ʽΪCH2=CHCOOCH2CH2COOH��E�����Ӿ۷�Ӧ����F��F�Ľṹ��ʽΪ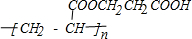 ���ٽ����Ŀ�������
���ٽ����Ŀ�������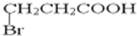 ��A����������ˮ��Һ����ʱ����ȡ����Ӧ��Ȼ���ữ����C��C�Ľṹ��ʽΪHOCH2CH2COOH��C����������Ӧ����G��G�Ľṹ��ʽΪOHCCH2COOH��C����������Ӧ���ɸ߷��ӻ�����H����ṹ��ʽΪ
��A����������ˮ��Һ����ʱ����ȡ����Ӧ��Ȼ���ữ����C��C�Ľṹ��ʽΪHOCH2CH2COOH��C����������Ӧ����G��G�Ľṹ��ʽΪOHCCH2COOH��C����������Ӧ���ɸ߷��ӻ�����H����ṹ��ʽΪ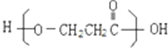 ��A��NaOH����Һ����ʱ��A������ȥ��Ӧ����B��B�Ľṹ��ʽΪCH2=CHCOONa��BȻ���ữ����D����D�Ľṹ��ʽΪCH2=CHCOOH��D��C��Ũ���������������������·�Ӧ����E��E�Ľṹ��ʽΪCH2=CHCOOCH2CH2COOH��E�����Ӿ۷�Ӧ����F��F�Ľṹ��ʽΪ
��A��NaOH����Һ����ʱ��A������ȥ��Ӧ����B��B�Ľṹ��ʽΪCH2=CHCOONa��BȻ���ữ����D����D�Ľṹ��ʽΪCH2=CHCOOH��D��C��Ũ���������������������·�Ӧ����E��E�Ľṹ��ʽΪCH2=CHCOOCH2CH2COOH��E�����Ӿ۷�Ӧ����F��F�Ľṹ��ʽΪ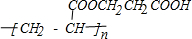 ��
��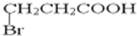 ���ʴ�Ϊ��
���ʴ�Ϊ��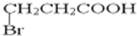 ��
��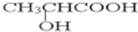 ��G�Ľṹ��ʽΪOHCCH2COOH��Ag�����ʵ���=
��G�Ľṹ��ʽΪOHCCH2COOH��Ag�����ʵ���=| 2.16g |
| 108g/mol |
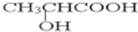 ��0.01mol��
��0.01mol��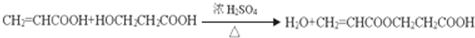 ��
��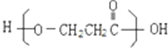 ��C�������۷�Ӧ����H����Ӧ����ʽΪ
��C�������۷�Ӧ����H����Ӧ����ʽΪ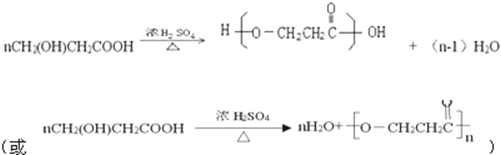 ��
��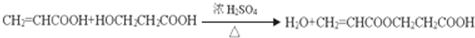 ��
�� ��
��


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������谷��Ħ������Ϊ126g |
| B��1mol�����谷������Ϊ126g |
| C�������谷��N����������Ϊ80% |
| D��1mol�����谷��15��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��v��NO��=0.1 mol?��L?s��-1 |
| B��v��NO��=0.02 mol?��L?s��-1 |
| C��v��NH3��=0.01 mol?��L?s��-1 |
| D��v��NH3��=0.2 mol?��L?s��-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
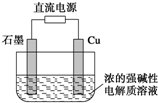 Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡCu2O�ĵ���ʾ��ͼ��ͼ������ܷ�ӦΪ2Cu+H2O
Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡCu2O�ĵ���ʾ��ͼ��ͼ������ܷ�ӦΪ2Cu+H2O
| ||
| A��ʯī�缫�ϲ������� |
| B��ͭ�缫������ԭ��Ӧ |
| C��ͭ�缫��ֱ����Դ�ĸ��� |
| D������0.1 mol����ת��ʱ����0.1 mol Cu2O���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����AΪFe��DΪ��������B�������ᣬҲ������ˮ |
| B����A��DΪ�����BΪˮ����C���������嵥�ʣ�Ҳ�����ǻ����� |
| C����A��B��C��D��Ϊ������÷�Ӧһ�����ڸ��ֽⷴӦ |
| D����A��B��C��D��Ϊ10����������C�ǿ�ʹʪ��ĺ�ɫʯ����ֽ���������壬��D �ڳ�����һ����Һ̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| A��Q1=Q2 | ||
B��
| ||
C��Q1��
| ||
D��Q1=
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B�������� |
| C������ | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ھ��ܻ����������ϰ�װͭ�ݶ� |
| B�����ŷź�ˮ�ĸ����������õ�������һ��ʯī��һͬ���뺣ˮ�� |
| C���ں�����������˿ϵסп����ں�ˮ�� |
| D���ڵ綯���ܵ��������Ͻ�ֱ����Դ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com