
| A. | c(Ba2+)、c(SO42-)均增大 | |
| B. | c(Ba2+)=c(SO42-)=[Ksp(BaSO4)]1/2 | |
| C. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)=Ksp(BaSO4) | |
| D. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)≠Ksp(BaSO4) |
分析 BaSO4饱和溶液中存在溶解平衡,BaSO4?Ba2++SO42-,溶度积的表达式K=c(Ba2+)×c(SO42-),溶度积K是温度的常数,只与温度有关,据此进行判断.
解答 解:A.BaSO4饱和溶液中存在溶解平衡,BaSO4?Ba2++SO42-,故c(Ba2+)=c(SO42-)且c(Ba2+)•c(SO42-)=Ksp(BaSO4).加入Na2SO4(s),Na2SO4溶于水中电离出SO42-使c(SO42-)增大,由于溶度积c(Ba2+)•c(SO42-)=Ksp(BaSO4)不变,则c(Ba2+)减小,故A错误;
B.根据A的分析可知,溶解平衡逆向移动,使c(Ba2+)减小,故c(Ba2+)<c(SO42-),故B错误;
C.溶度积是温度的常数,故达到平衡时溶度积不变,仍然为c(Ba2+)•c(SO42-)=Ksp(BaSO4),且c(Ba2+)<c(SO42-),故C正确;
D.溶度积是温度的常数,故达到平衡时溶度积不变,仍然为c(Ba2+)•c(SO42-)=Ksp(BaSO4),故D错误;
故选C.
点评 本题考查了溶解平衡及其影响,题目难度不大,明确难溶物溶解平衡及其影响因素为解答关键,注意溶度积只与溶质类型、温度有关,与浓度大小无关,试题培养了学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
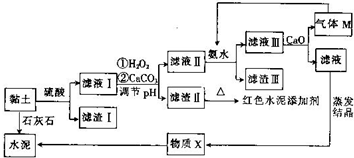
| Fe(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀时的pH | 6.3 | 1.9 | 3.4 |
| 完全沉淀时的pH | 8.3 | 3.2 | 4.7 |
 ;向滤液Ⅲ中加入CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
;向滤液Ⅲ中加入CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
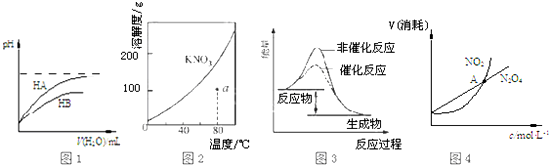
| A. | 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH | |
| B. | 图2表示 KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3的不饱和溶液 | |
| C. | 图3 表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| D. | 图4表示恒温恒容条件下,2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
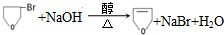 .
.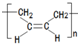 .
. .
.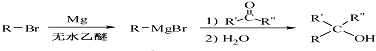
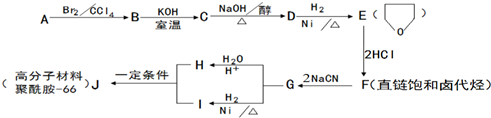
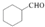 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: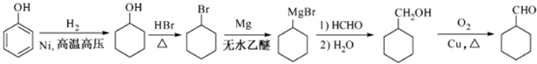 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
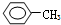
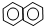
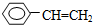
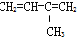
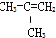
| A. | ④和⑥ | B. | ①、②和③ | C. | ⑤和⑦ | D. | ⑥和⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
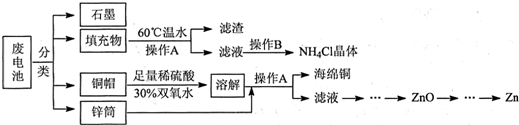
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ④⑤ | C. | ③④⑤ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
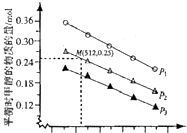
| 化学键 | C=0 | H-H | C-C | C-H | 0-H | C-0 |
| 键能/kJ•mol-1 | 803 | 436 | 332 | 409 | 463 | 326 |
| 成分 | 含量/(mg/L) | 成分 | 含量(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3-; | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com