
【题目】已知: ![]() 溶液是检验
溶液是检验![]() 的试剂,若溶液中存在
的试剂,若溶液中存在![]() ,将产生蓝色沉淀。将
,将产生蓝色沉淀。将![]() 的KI溶液和
的KI溶液和![]()
![]() 溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“
溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“![]() ”的是
”的是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入 | 有黄色沉淀生成 |
③ | 滴入 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A. ① B. ②和④ C. ③和④ D. ①和②
【答案】A
【解析】将0.2molL-1的KI溶液和0.05molL-1 Fe2(SO4)3溶液等体积混合后,I-过量,若不是可逆反应,Fe3+全部转化为Fe2+,则溶液中无Fe3+,故只需要证明溶液中含Fe3+,则即能证明此反应为可逆反应,能建立化学平衡。①向溶液中滴入KSCN溶液,溶液变红,则说明溶液中有Fe3+,即能说明反应存在平衡,故①正确;②向溶液中滴入AgNO3溶液有黄色沉淀生成,溶液中I-过量,无论是否存在平衡反应,都会有黄色沉淀生成,所以不能说明反应存在平衡,故②错误;③无论反应存不存在平衡,溶液中均存在Fe2+,滴入K3[Fe(CN)6]溶液均有蓝色沉淀生成,故③错误;④无论反应存不存在平衡,溶液中均有I2,滴入淀粉溶液后溶液均变蓝色,故不能证明存在平衡,故④错误;故选A。


科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”。下列做法不利于保护环境的是( )
A.推广使用电动汽车等低碳交通工具
B.推广垃圾分类,电子设备以旧换新
C.用生物方法脱除生活污水中的氮和磷
D.加大铅酸蓄电池、含汞锌锰等电池的生产
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B为单质,C为化合物。
![]()
能实现上述转化关系的是
①若C溶于水后得到强碱溶液,则A可能是Na
②若C的溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A. ①② B. ②④ C. ①③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电化学原理,将NO2、O2 和熔融KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72-废水,如下图所示; 电解过程中溶液发生反应:Cr2O72-+ 6Fe2++ 14H+ = 2Cr3++ 6Fe3+ + 7H2O
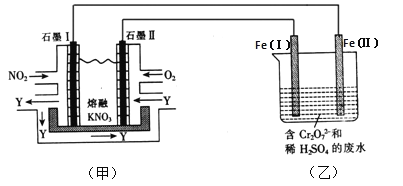
(1)甲池工作时,NO2转变成绿色硝化剂Y,Y 是N2O5,可循环使用。则石墨II 是电池的____极;石墨Ⅰ附近发生的电极反应式为________________。
(2)工作时,甲池内的NO3-离子向__________极移动(填“石墨I”或“石墨II”); 在相同条件下,消耗的 O2和NO2的体积比为________________。
(3)乙池中Fe( I)棒上发生的电极反应为___________________。
(4)若溶液中减少了0.01mol Cr2O72-,则电路中至少转移了___________________mol 电子。
(5)向完全还原为Cr3+的乙池工 业废水中滴加NaOH 溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3 存在以下 溶解平衡:Cr(OH)3(s) = Cr3+(aq) + 3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c(OH-)=1.0 ×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH 应调至_____。比色卡对照即可。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:
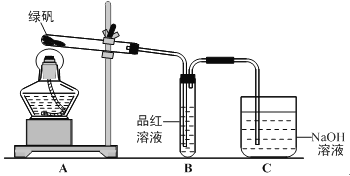
(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是 ,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是 。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中 。(填字母)
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解气态产物的装置:
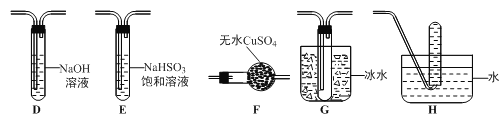
①丙组同学的实验装置中,依次连接的合理顺序为 。
②能证明绿矾分解产物中有O2的实验操作及现象是 。
(4)为证明绿矾分解产物中含有三价铁,选用的实验仪器有试管、胶头滴管、 ;选用的试剂为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烷烃按沸点由高到低顺序排列正确的是( )
①正丁烷②异丁烷③正戊烷④异戊烷⑤新戊烷
A.①②③④⑤B.⑤④③②①C.③①⑤④②D.③④⑤①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示装置的说法错误的是( )
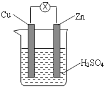
A. 锌片发生氧化反应
B. 铜片周围溶液变为蓝色
C. 电子由锌片通过外电路流向铜片
D. 溶液中SO42-向负极方向流动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为化合物,且其摩尔质量为95g·mol-1,D为混合物,M是一种常见的气体,N是一种常见金属单质。它们之间的转化如图所示。
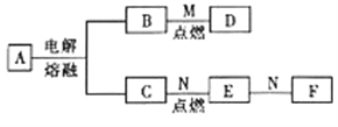
请回答下列问题:
(1)A的化学式为___________。
(2)由A生成B和C的反应中,每转移1mol电子,可以生成________gB。
(3)已知D中含有两种固体,且其中有一种固体单质为黑色,另一种固体为B的氧化物。则M的摩尔质量为_________g·mol-1。
(4)E的水溶液与N反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用水钴矿(主要成分为Co2O3,还含少量Fe2O3、 Al2O3、MgO、CaO等杂质) 制备钴的氧化物,其制备工艺流程如下:
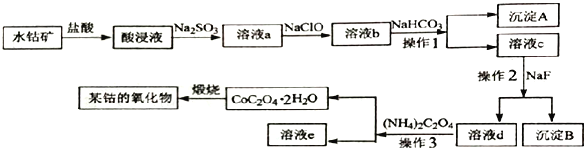
回答下列问题:
(1)在加入盐酸进行“酸浸”时,能提高“酸浸”速率的方法有______________(任写一种)。
(2)“酸浸”后加入Na2SO3,钴的存在形式为Co2+,写出产生Co2+反应的离子方程式_______________________________。
(3)溶液a中加入NaClO的作用为_______________________________。
(4)沉淀A 的成分为__________________。操作2的名称是___________________。
(5)已知: Ksp (CaF2)=5.3×10-9,Ksp(MgF2)=5.2×10-12,若向溶液c 中加入NaF溶液,当Mg2+恰好沉淀完全即溶液中c(Mg2+)=1.0×10-5moI/L,此时溶液中c(Ca2+)最大等于_________mol·L-1。
(6)在空气中煅烧CoC2O4 生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05 g,CO2的体积为6.72 L(标准状况),则此反应的化学方程式为_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com