
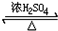 CH3COOCH(CH3)2+H2O,取代反应或酯化反应反应类型
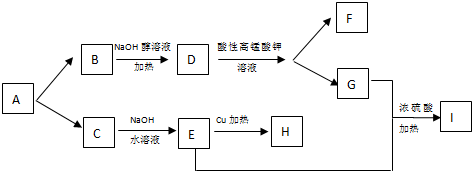
CH3COOCH(CH3)2+H2O,取代反应或酯化反应反应类型分析 烷烃的化学式为CnH2n+2,根据燃烧方程式:CnH2n+2+(n+$\frac{2n+2}{4}$)O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O来进行计算气态烷烃A的化学式C3H8,A的一氯代物有两种同分异构体分别为B和C,CH3CH2CH2Cl、CH3CHClCH3,C在氢氧化钠的水溶液中取代,生成醇E,E催化氧化生成H,但H不能发生银镜反应,说明H为酮,则E为(CH3)2CHOH,逆推C为CH3CHClCH3,B为CH3CH2CH2Cl,B能在氢氧化钠的醇溶液中消去,D为CH3CH=CH2,D被酸性高锰酸钾氧化,E为醇,G+E能发生酯化反应,所以G为羧酸,G为CH3COOH,F为二氧化碳,据此分析解答.
解答 解:标况下取22.4L该烃的物质的量为n=$\frac{V}{{V}_{m}}$=$\frac{22.4L}{22.4L/mol}$=1mol,氧气的质量是160g,物质的量为n=$\frac{m}{M}$=$\frac{160g}{32g/mol}$=5mol,烷烃的化学式为CnH2n+2,
CnH2n+2+(n+$\frac{2n+2}{4}$)O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O,
1 n+$\frac{2n+2}{4}$
1 5
则有:n+$\frac{2n+2}{4}$=5,解得n=3,故烷烃化学式为C3H8,结构简式只有一种:CH3CH2CH3,A的一氯代物有两种同分异构体分别为B和C,CH3CH2CH2Cl、CH3CHClCH3,C在氢氧化钠的水溶液中取代,生成醇E,E催化氧化生成H,但H不能发生银镜反应,说明H为酮,则E为(CH3)2CHOH,逆推C为CH3CHClCH3,B为CH3CH2CH2Cl,B能在氢氧化钠的醇溶液中消去,D为CH3CH=CH2,D被酸性高锰酸钾氧化,E为醇,G+E能发生酯化反应,所以G为羧酸,G为CH3COOH,F为二氧化碳,
A→B:CH3CH2CH3+Cl2 $\stackrel{光照}{→}$CH3CH2CH2Cl+HCl,
B→D:CH3CH2CH2Cl+NaOH$→_{△}^{醇}$CH3CH=CH2↑+NaCl+H2O,
E→H:2(CH3)2CHOH+O2 $→_{△}^{Cu}$2CH3COCH3+2H2O,
G+E→I:(CH3)2CHOH+CH3COOH 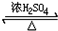 CH3COOCH(CH3)2+H2O,
CH3COOCH(CH3)2+H2O,
(1)该烃1mol,氧气5mol,根据燃烧方程式:CnH2n+2+(n+$\frac{2n+2}{4}$)O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O,计算得气态烷烃A的化学式C3H8,结构简式只有一种:CH3CH2CH3,根据H不能发生银镜反应,说明H为酮,逆推C为CH3CHClCH3,
故答案为:CH3CH2CH3;CH3CHClCH3;
(2)根据以上分析,A→B为烷烃的取代,B→D为卤代烃的消去,E→H为醇的催化氧化,G+E→I为酸和醇的酯化反应,也为取代反应,
故答案为:CH3CH2CH3+Cl2 $\stackrel{光照}{→}$CH3CH2CH2Cl+HCl,取代反应;CH3CH2CH2Cl+NaOH$→_{△}^{醇}$CH3CH=CH2↑+NaCl+H2O,消去反应;2(CH3)2CHOH+O2 $→_{△}^{Cu}$2CH3COCH3+2H2O,氧化反应;(CH3)2CHOH+CH3COOH 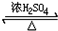 CH3COOCH(CH3)2+H2O,取代反应或酯化反应;
CH3COOCH(CH3)2+H2O,取代反应或酯化反应;
(3)H为CH3COCH3,其同分异构体的结构简式为CH3CH2CHO,该同分异构体与银氨溶液反应的化学方程式为:CH3CH2CHO+2[Ag(NH3)2]OH $\stackrel{水浴}{→}$CH3CH2COOH+2Ag↓+3NH3↑+H2O,
故答案为:CH3CH2CHO+2[Ag(NH3)2]OH $\stackrel{水浴}{→}$CH3CH2COOH+2Ag↓+3NH3↑+H2O.
点评 本题考查有机推断,涉及烯烃、醇、醛、羧酸等性质以及学生推理能力等,是对有机化合物知识的综合考查,能较好的考查考生的思维能力,推出A的分子式,H不能发生银镜反应,判断H为酮,以此推出其它物质的结构是解题的关键,题目难度中等,是高考热点题型.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
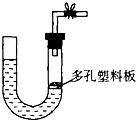 如图是气体制取装置,下列能用此装置制取气体并能“随开随用、随关随停”的是( )
如图是气体制取装置,下列能用此装置制取气体并能“随开随用、随关随停”的是( )| A. | 大理石和稀硫酸制取二氧化碳 | B. | 锌粒和稀硫酸制氢气 | ||
| C. | 块状碳酸钠和稀盐酸制取二氧化碳 | D. | 氯酸钾和二氧化锰制氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
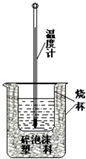 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度(t2)℃ | 温差(t2-t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.0 | 3.0 |
| 2 | 25.1 | 25.1 | 25.1 | 28.2 | 3.1 |
| 3 | 25.1 | 25.1 | 25.1 | 28.3 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应” | |
| B. | 将垃圾分类并回收利用是垃圾处理的发展方向 | |
| C. | 废旧电池的回收,其主要目的是保护环境,而不是回收金属 | |
| D. | 淀粉餐具被认为是有发展前景的一次性餐具,可有利于保护环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素编号 | 元素性质或原子结构 |
| T | 单质是一种淡黄色固体,是黑火药成分之一 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
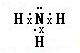 ,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com