
| A. | 2molCl2 | B. | 3.01×1023个氧分子 | ||
| C. | 2g氢气 | D. | 标准状况下,11.2LHe |
科目:高中化学 来源: 题型:选择题
| A. | c(H+) | B. | Ka(HF) | C. | $\frac{c({F}^{-})}{c({H}^{+})}$ | D. | $\frac{c({H}^{+})}{c(HF)}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X可能是( )| A. | ①②③④ | B. | ①③④⑤ | C. | ③④⑤⑦ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCaC2中含有阴离子数目为2NA | |
| B. | 向FeI2溶液中通入氯气,当有2molFe2+被氧化时,转移电子的数目为2NA | |
| C. | 2.8g乙烯与丙烯的混合物中含碳原子的数目为0.4NA | |
| D. | 用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移电子数目为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水溶液:Na+、K+、NO3-、CH3CHO | |
| B. | 氢氧化钠溶液:AlO2-、K+、Cl-、NO3- | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Cl- | |
| D. | 高锰酸钾溶液:H+、Na+、SO42-、CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在同温同压下,22.4L的任何气体都是1 mol | |
| B. | 1molCaCl2完全溶于水后,可以得到1 mol Ca2+和2 mol Cl- | |
| C. | 在标准状况下,11.2 L某气体的质量为22 g,则该气体的相对分子质量是44 g/mol | |
| D. | 将80g NaOH固体溶于1 L水中,所得溶液中NaOH的物质的量浓度是2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤⑥ | C. | ②③④ | D. | ①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
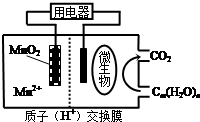
| A. | 分子组成为Cm (H2O)n的物质一定是糖类 | |
| B. | 正极反应式为:MnO2+4H++2e-=Mn2++2H2 O | |
| C. | 放电过程中,H+从正极区移向负极区 | |
| D. | 若Cm (H2O)n是葡萄糖,当电路中转移了6NA电子时,反应的葡萄糖质量是60g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com