
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量49 6kJ,水蒸气中1molH-O键形成时放出热量463kJ,则氢气中1molH-H键断裂时吸收热量为( )
6kJ,水蒸气中1molH-O键形成时放出热量463kJ,则氢气中1molH-H键断裂时吸收热量为( )
A.920kJ B.557kJ C.436kJ D.188kJ
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:2016-2017学年吉林省高二上学期9月月考化学试卷(解析版) 题型:选择题
在碱性锌锰干电池中,已知氢氧化钾为电解质,发生的电池总反应为:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。下列该电池的电极反应,正确的是( )
A.负极反应为Zn-2e-===Zn2+
B.负极反应为Zn+2H2O-2e-===Zn(OH)2+2H+
C.正极反应为2MnO2+2H++2e-===2MnOOH
D.正极反应为2MnO2+2H2O+2e-===2MnOOH+2OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次段考化学卷(解析版) 题型:选择题
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) 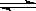 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
A.该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变
B.因该反应熵变(△S)大于0,焓变(△H)大于0,所以在低温下自发进行
C.根据表中数据,计算15.0℃时的分解平衡常数约为2.0×10-9(mol·L-1)3
D.达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北大附中河南分校高二上第一次月考化学卷(解析版) 题型:选择题
在密闭容器里,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知3v(B)=2v(A)、2v(C)=3v(B),则此反应可 表示为( )
表示为( )
A.2A+3B = 2C B.A+3B = 2C C.3A+2B = 3C D.A+B = C
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北大附中河南分校高二上第一次月考化学卷(解析版) 题型:选择题
关于化学反应与能量的说法正确的是( )
A.化学键断裂需要吸收能量
B.化学反应中能量变化的大小与反应物的质量多少无关
C.在化学反应过程中反应物的总能量总是等于生成物的总能量
D.放热反应都能自发进行,吸热反应需要在加热的条件下才能进行
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北大附中河南分校高二上第一次月考化学卷(解析版) 题型:选择题
根据盖斯定律判断如下图所示的物质转变过程中,正确的是( )
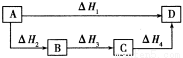
A.ΔH1=ΔH2=ΔH3=ΔH4 B.ΔH1+ΔH2=ΔH3+ΔH4
C.ΔH1+ΔH2+ΔH3=ΔH4 D.ΔH1=ΔH2+ΔH3+ΔH4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学卷(解析版) 题型:选择题
维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。近年来,科学家发现维生素C有防癌作用。下列关于维生素C的说法中错误的是(双选)……( )
A、维生素C是氧化 物
物
B、维生素C由6个碳元素、8个氢元素、6个氧元素组成
C、维生素C中C、H、O三种元素的质量 比为9:1:12
比为9:1:12
D、青少年应多吃蔬菜水果,切忌偏食
查看答案和解析>>
科目:高中化学 来源:2016-2017年河北定州中学承智班高二上第一次月考化学卷(解析版) 题型:选择题
下列有关物质用途的说法错误的是
A.可用铝槽密闭盛装浓硫酸
B.工业上利用蛋白质的水解反应生产肥皂和甘油
C.乙醇可用作汽车燃料
D.食醋可用于消除暖水瓶中的水垢
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:实验题
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 .
②某学生设计回收四氯化碳的操作为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体;
d.将分液漏斗充分振荡后静置
其中分液漏斗使用前须进行的操作是 ,上述操作正确的顺序是 (填序号)
(3)已知:I2+2S2O32﹣═2I﹣+S4O62﹣.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10﹣3mol· L﹣1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示) mg/kg。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com