
| 0.001cVmol |
| 0.025L |


科目:高中化学 来源: 题型:
| A、②③⑥ | B、①③④⑤⑥ |
| C、①②③⑥ | D、①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
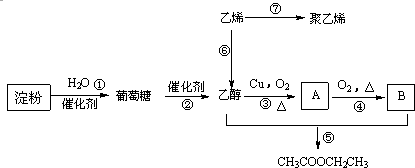
查看答案和解析>>
科目:高中化学 来源: 题型:
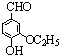 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.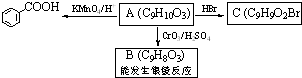
| CtO2/H2SO4 |
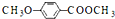 )是一种医药中间体.请设计合理方案用茴香醛(
)是一种医药中间体.请设计合理方案用茴香醛( )合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)
)合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)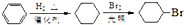
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可逆反应不可以自发进行 |
| B、催化剂可以加块反应速率,也可增大反应物的转化率 |
| C、当有多个反应参加时,使用催化剂,可增加目标产物的产率 |
| D、H2与O2点燃生成H2O,H2O电解产生H2与O2,说明该反应可逆 |
查看答案和解析>>
科目:高中化学 来源: 题型:
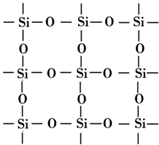 制造光导纤维的材料是一种很纯的硅氧化物,它是具有立体网状结构的晶体,下图是简化了的平面示意图,关于这种制造光纤的材料,下列说法正确的是( )
制造光导纤维的材料是一种很纯的硅氧化物,它是具有立体网状结构的晶体,下图是简化了的平面示意图,关于这种制造光纤的材料,下列说法正确的是( )| A、它的晶体中硅原子与氧原子数目比是1:4 |
| B、它的晶体中硅原子与氧原子数目比是1:6 |
| C、这种氧化物是原子晶体 |
| D、这种氧化物是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B、单质硅是将太阳能转变为电能的常用材料 |
| C、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| D、某溶液中加入足量稀盐酸无明显现象,再加入BaCl2溶液产生白色沉淀,该溶液中一定含有SO42-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑤ | B、①②③⑤ |
| C、①②③ | D、①② |
查看答案和解析>>
科目:高中化学 来源: 题型:
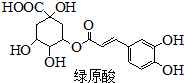 绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )| A、奎尼酸分子式为C7H12O6 |
| B、1mol奎尼酸与NaOH溶液反应,最多消耗5molNaOH |
| C、绿原酸能发生取代、加成、消去和缩聚反应 |
| D、咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com