
| A. | NO2 是无色气体 | |
| B. | NO2 能用排水气法收集 | |
| C. | NO2能与水反应,在反应中氮元素的化合价不发生变化 | |
| D. | NO2能与水反应,在反应中NO2既是氧化剂,又是还原剂 |
分析 A.二氧化氮为红棕色气体;
B.二氧化氮和水发生反应;
C.该反应中,N元素的化合价既升高又降低,氮元素化合价+4价变化为+5价和+2价;
D.该反应中,N元素的化合价既升高又降低,NO2既是氧化剂又是还原剂.
解答 解:A.二氧化氮是红棕色气体,故A错误;
B.3NO2+H2O=2HNO3+NO,二氧化氮和水反应,不能排水法收集,故B错误;
C.反应中3NO2+H2O=2HNO3+NO,氮元素化合价+4价变化为+5价和+2价,发生了氧化还原反应,故C错误;
D.NO2能与水反应,N元素的化合价既升高又降低,NO2既是氧化剂又是还原剂,故D正确;
故选D.
点评 本题考查物质性质、氧化还原反应,明确元素的化合价变化是解答本题的关键,注意氧化剂、还原剂的概念及判断来解答,题目难度中等.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:4 | B. | 3:11 | C. | 1:11 | D. | 21:22 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
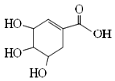
| A. | 分子式为C7H6O5 | B. | 分子中含有两种官能团 | ||
| C. | 1mol该有机物能与4molNaOH反应 | D. | 可发生加成和取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵和草木灰混合使用,能增强化肥的肥效 | |
| B. | 二氧化硫和漂白粉混合使用,能增强漂白效果 | |
| C. | 浓盐酸和高锰酸钾混合使用,能增强高锰酸钾的氧化性 | |
| D. | 氢氧化钠固体和氧化钙混合使用,能增加吸水能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把金属铁放入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将氢氧化铁放入盐酸中:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 氢氧化钡跟硫酸铜溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 石灰石跟盐酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
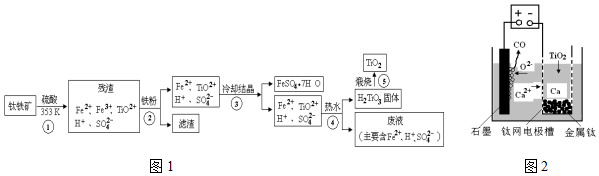
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个H+的质量为1 g | |
| B. | 2 L 0.5 mol/L Na2SO4溶液中含NA个Na+ | |
| C. | 32 g O2中含有2NA个氧原子 | |
| D. | 标准状况下,1 mol H2O中含有NA个分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com