
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol•L-1 NaOH溶液 | 50 mL 0.5 mol•L-1 HCl溶液 | 20℃ | 23.3℃ | -56.8kJ/mol |
| ② | 50 mL 0.55 mol•L-1 NaOH溶液 | 50 mL 0.5 mol•L-1 HCl溶液 | 20℃ | 23.5℃ | |
分析 (1)根据中和热测定的实验步骤选用需要的仪器,然后判断还缺少的仪器;
(2)①金属导热快,热量损失多;
②中和热测定实验成败的关键是保温工作;
(3)先判断温度差的有效性,然后求出温度差平均值,再根据Q=m•c•△T计算反应放出的热量,然后根据△H=-$\frac{Q}{n}$kJ/mol计算出反应热;
(4)①弱电解质电离吸热;
②反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答.
解答 解:(1)中和热的测定过程中,需要用量筒量取酸溶液、碱溶液的体积,需要使用温度计测量温度,测量过程中用玻璃棒不断搅拌,所以还缺少玻璃用品是温度计、环形玻璃搅拌棒;
故答案为:温度计、环形玻璃搅拌棒;
(2)①不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为铜是热的良导体,热量损失大;
故答案为:否;铜是热的良导体,有热量散失;
②中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失;
故答案为:保温,减少热量散失;
(3)2次温度差分别为:3.3℃,3.5℃,第2组数据都有效,温度差平均值=3.4℃,50mL0.55mol•L-1NaOH和50mL.0.5mol•L-1HCl质量和为m=100mL×1g/mL=100g,c=4.18J/(g•℃),△T=3.4℃,代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g•℃)×100g×3.4℃=1421.2J=1.4212kJ,即生成0.025mol的水放出热量1.4212kJ,所以生成1mol的水放出热量为$\frac{1.4212kJ×1mol}{0.025mol}$=56.8kJ,即该实验测得的中和热△H=-56.8kJ/mol;
故答案为:-56.8;
(4)①醋酸为弱酸,电离过程为吸热过程,所以醋酸(CH3COOH)代替HCl溶液反应,反应放出的热量偏小;
故答案为:偏小;
②反应放出的热量和所用酸以及碱的量的多少有关,若用60mL 0.5mol•L-1HCl溶液与50mL 0.55mol•L-1NaOH溶液完成实验,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL 0.5mol•L-1HCl溶液与50mL 0.55mol•L-1NaOH溶液进行实验,测得中和热数值相等;
故答案为:偏大;不变.
点评 本题考查了中和热的测定方法,题目难度中等,明确中和热的测定步骤为解答关键,注意掌握中和热计算方法,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 立方烷( 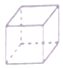 )的六氨基(-NH2)取代物有3种 )的六氨基(-NH2)取代物有3种 | |
| B. | C3H7ClO(有羟基)的同分异构体数目有5种 | |
| C. | 甲苯与氢气充分加成后的一溴代物有4种 | |
| D. | 分子式为C5H10O2的有机物中能与NaOH溶液反应的有13种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -332 | B. | -118 | C. | 350 | D. | 130 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,向100gNaOH饱和溶液中加入0.39gNa2O2固体,恢复到常温,NaOH溶液的物质的量浓度一定不变 | |
| B. | 向一恒容容器中充入lmolN2和lmolH2,在一定条件下反应并达到平衡.升温,再次达到平衡状态,N2的体积分数一定不变 | |
| C. | 向50mL0.55mol/L的NaOH溶液中加入50mL0.50mol/L的稀盐酸,测定中和热,继续加入6mL等浓度的稀盐酸,测定的中和热一定不变 | |
| D. | 将2.3gNa投入100mL水中,产生H2,若在反应前向水中加入100 mL煤油,则产生H2的速率一定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断 裂时需要吸收的能量/kJ | 436 | 230 | 369 |
| A. | 404 | B. | 72 | C. | 230 | D. | 200 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,35.5g的氯气与足量的氢氧化钙溶液完全反应,转移的电子数为0.5NA | |
| B. | 60g甲酸甲酯和葡萄糖的混合物含有的碳原子数目为2NA | |
| C. | 标准状况下,2.24L PH3与3.4gH2S气体分子所含电子数目均为1.8NA | |
| D. | 已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,当该反应生成NA个NH3分子时,反应放出的热量小于46.2kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com