
| A、196kJ |
| B、98kJ |
| C、<196kJ |
| D、>196kJ |


科目:高中化学 来源: 题型:
| 选项 | 待提纯物 | 杂质 | 试剂及主要操作方法 |
| A | 苯 | 溴单质 | 加苯酚,过滤 |
| B | 甲苯 | 苯甲酸 | 饱和NaHCO3溶液,分液 |
| C | 甲烷 | 乙烯 | 通入酸性高锰酸钾溶液,洗涤 |
| D | 乙醛 | 乙酸 | 加入氢氧化钠溶液,分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、180mL | B、120mL |
| C、90mL | D、60mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用上如图模拟工业上电解精炼锡.装置如图所示(C、D电极为石墨电极):
用上如图模拟工业上电解精炼锡.装置如图所示(C、D电极为石墨电极):查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
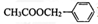 )对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成线路如下:
)对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成线路如下: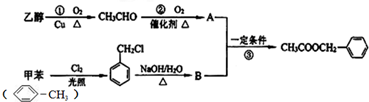
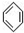 b.
b.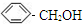 c.
c.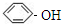 d.
d.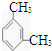
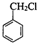 c.2CH3CHO+O2
c.2CH3CHO+O2| 催化剂 |
| △ |
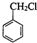 )在催化剂作用下反应制备.
)在催化剂作用下反应制备.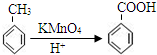
| Cl2 |
| 光照 |
| NaOH溶液 |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com