
【题目】在恒容密闭容器中进行反应:X2(g)+3Y2(g) ![]() 2Z2(g),若X2、Y2、Z2的初始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,当反应达到平衡后,各物质的浓度有可能是
2Z2(g),若X2、Y2、Z2的初始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,当反应达到平衡后,各物质的浓度有可能是
A.X2为0.2 mol·L-1 B.Y2为0.1 mol·L-1
C.Z2为0.4mol·L-1 D.Y2为0.6 mol·L-1
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】现有三组溶液: ①KNO3和NaCl溶液 ②H2O和C2H5OH(乙醇) ③Br2的CCl4溶液,以上各混合液的分离方法依次是
A.分液、蒸馏、萃取 B.结晶、蒸馏、萃取
C.结晶、蒸馏、蒸馏 D.过滤、蒸馏、萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示。已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N![]() N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是
N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是

A. N4属于一种新型的化合物
B. N4分子中存在非极性键
C. N4分子中N—N键角为109°28′
D. 1 mol N4转变成N2将吸收882 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备乙酸乙酯的装置,如图所示,回答下列问题:
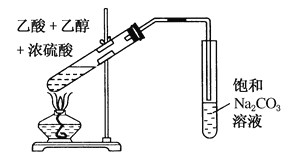
(1)乙醇、乙酸和浓硫酸混合时,应为_______________________________________。
(2)收集乙酸乙酯的试管内盛有的饱和碳酸钠溶液的作用是_________________________。
(3)反应中浓硫酸的作用是________________________________。
(4)反应中乙醇和乙酸的转化率不能达到100%,原因是__________________________。
(5)将收集到的乙酸乙酯分离出来的方法为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在压强为0.1 MPa、10L恒容的密闭容器中, 将2 mol CO与 5 mol H2的混合气体在催化剂作用下能生成甲醇:CO(g) + 2H2(g)![]() CH3OH(g) △H<0 请回答下列问题:
CH3OH(g) △H<0 请回答下列问题:
(1)①该反应的熵变ΔS__________0(填“>”、“<”或“=”)。
②若温度T1 >T2,则平衡常数K(T1)___________K(T2)(填“大于”、“小于”或“等于”)
③下列措施既可加快反应速率又可增加甲醇产率的是__________;
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入2 mol CO和5 mol H2
④下列可说明反应已达到化学平衡状态的是________;
A.v生成(CH3OH)=v消耗(CO) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.CO与H2浓度比不再变化
(2)若温度T2时,5min后反应达到平衡,CO的转化率为75%,则:
①平衡时体系总的物质的量为________mol;
②反应的平衡常数K=______________;
③反应在0-5min区间的平均反应速率v(H2)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)( )
A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2 +2OH-=== Cl-+ ClO-+ H2O
B.该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C.该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2 ↑+ H2O
D.该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+ CH3COO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol的镁、铝混合物溶于100 mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。

当V1=160mL时,则金属粉末中n(Mg)=________ mol,V2=_____________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) _____________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )。
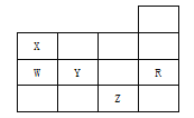
A. 常压下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. Y的氢化物的沸点比H2O的沸点高
D. Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在4种离子:NO3-、SO42-、Mg2+、Na+,其中SO42-、Mg2+、Na+ 物质的量之比为1:2:2,则NO3-与SO42-物质的量之比为( )
A.1:2 B.3:1 C.4:1 D.2:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com