
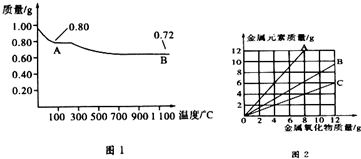
| A. | 图1中产物A、B的化学式分别为Cu2O和CuO | |
| B. | 图1整个过程中共生成0.26g水 | |
| C. | 图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是C | |
| D. | 图1中,A到B过程中有0.01 mol电子发生了转移 |
分析 0.98 g Cu(OH)2的物质的量为$\frac{0.98g}{98g/mol}$=0.01 mol,若完全分解得到CuO,由Cu元素守恒,n(CuO)=0.01 mol,m(CuO)=0.01mol×80g/mol=0.8g,若完全分解得到Cu2O,由Cu元素守恒,n(Cu2O)=$\frac{0.01mol}{2}$=0.005mol,m(Cu2O)=0.005mol×144g/mol=0.72g,故A为CuO、B为Cu2O,
A.由上述分析可知,A为CuO、B为Cu2O;
B.根据H元素守恒计算水的物质的量,再根据m=nM计算生成水的质量;
C.根据CuO的化学式计算CuO中所含Cu元素的质量与CuO的质量之比,结合图象判断;
D.由A点到B点发生反应:4CuO$\frac{\underline{\;高温\;}}{\;}$2Cu2O+O2↑,CuO完全分解为Cu2O,结合Cu元素化合价变化计算转移电子.
解答 解:0.98 g Cu(OH)2的物质的量为$\frac{0.98g}{98g/mol}$=0.01 mol,若完全分解得到CuO,由Cu元素守恒,n(CuO)=0.01 mol,m(CuO)=0.01mol×80g/mol=0.8g,若完全分解得到Cu2O,由Cu元素守恒,n(Cu2O)=$\frac{0.01mol}{2}$=0.005mol,m(Cu2O)=0.005mol×144g/mol=0.72g,故A为CuO、B为Cu2O,
A.由上述分析可知,A为CuO、B为Cu2O,故A错误;
B.根据H元素守恒,生成水的物质的量为:$\frac{0.01mol×2}{2}$=0.01mol,故生成水的质量为:0.01mol×18g/mol=0.18g,故B错误;
C.根据CuO的化学式可知CuO中所含Cu元素的质量与CuO的质量之比=64:80=4:5,即曲线斜率为0.8,曲线A的斜率大于1,曲线C的斜率为0.5,曲线B的斜率为0.8,故曲线B表示表示CuO和其中所含Cu元素质量关系,故C错误;
D.由A点到B点发生反应:4CuO$\frac{\underline{\;高温\;}}{\;}$2Cu2O+O2↑,CuO完全分解为Cu2O,Cu元素化合价由+2价降低为+1价,故转移电子为0.01mol×(2-1)=0.01mol,故D正确;
故选D.
点评 本题考查混合物反应的计算,为高频考点,题目难度中等,把握极限法判断A、B对应的物质是解题关键,试题侧重分析、计算能力的综合考查.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L就是气体摩尔体积 | |
| B. | 标准状况下,22.4L任何物质都含有大约6.02×1023个分子 | |
| C. | 非标准状况下,1mol任何气体的体积不可能为22.4L | |
| D. | 1mol氢气和氧气的混合气体在标准状况下的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 反应温度/℃ | 800 | 800 | 850 |
| c(A)起始/mol•L-1 | 1 | 2 | 1 |
| c(A)平衡/mol•L-1 | 0.5 | 1 | 0.85 |
| 放出的热量/kJ | a | b | c |
| A. | 实验Ⅲ的化学平衡常数K<1 | |
| B. | 实验放出的热量关系为b=2a | |
| C. | 实验Ⅲ在30 min达到平衡,30 min内A的速率:v(A)=0.002 5 mol•L-1•min-1 | |
| D. | 当容器内气体密度不随时间而变化时上述反应达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| SrSO4 | BaSO4 | Sr(OH)2 | Fe(OH)3 | Fe(OH)2 | |
| Ksp | 3.3×10-7 | 1.1×10-10 | 3.2×10-4 | 2.6×10-39 | 4.87×10-17 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
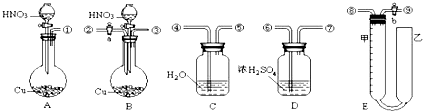
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2s22p2和2s22p4 | B. | 3s23p4和2s22p4 | C. | 3s2和2s22p5 | D. | 3s1和3s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C10H16 | B. | C11H14 | C. | C12H18 | D. | C13H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com