
| A. | 碳酸氢铵溶液和足量氢氧化钠溶液混合的离子反应:HCO3-+OH-═CO32-+H2O | |
| B. | 等物质的量浓度、等体积的氨水和盐酸混合后:c(NH4+)═c(Cl-) | |
| C. | 0.1 mol•L-1氨水加水稀释,c(NH4+)与c(H+)的比值将减小 | |
| D. | pH=8的0.1 mol•L-lNaX溶液中,由水电离出的c(OH-)=1×10-8mol•L-1 |
分析 A.碳酸氢铵和足量氢氧化钠溶液反应铵根也会结合氢氧根离子生成一水合氨;
B.等物质的量浓度、等体积的氨水和盐酸混合后恰好反应生成氯化铵溶液,铵根离子水解溶液显酸性,结合电荷守恒分析判断;
C.0.1 mol•L-1氨水加水稀释,促进一水合氨的电离,铵根、氢氧根离子物质的量浓度减小,氢离子物质的量浓度增大;
D.pH=8的0.1 mol•L-lNaX溶液中,X-离子水解结合水电离出的氢离子,促进水电离平衡正向进行,溶液显碱性,氢氧根离子是水完全电离出的离子;
解答 解:A.碳酸氢铵和足量氢氧化钠溶液反应铵根也会结合氢氧根离子生成一水合氨,反应的离子方程式为:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故A错误;
B.等物质的量浓度、等体积的氨水和盐酸混合后恰好反应生成氯化铵溶液,铵根离子水解溶液显酸性,C(H+)>c(OH-),溶液中电荷守恒分析,C(H+)+c(NH4+)=c(OH-)+c(Cl-),得到c(NH4+)<c(Cl-),故B错误;
C.0.1 mol•L-1氨水加水稀释,促进一水合氨的电离,铵根、氢氧根离子物质的量浓度减小,溶液中离子积常数可知氢离子物质的量难度增大,$\frac{c(N{{H}_{4}}^{+})}{c({H}^{+})}$比值减小,故C正确;
D.pH=8的0.1 mol•L-lNaX溶液中,X-离子水解结合水电离出的氢离子,促进水电离平衡正向进行,溶液显碱性,氢氧根离子是水完全电离出的离子,由水电离出的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-8}}$=1×10-6mol•L-1,故D错误;
故选C.
点评 本题考查了离子反应、弱电解质电离平衡的影响因素、盐类水解平衡的理解应用,掌握基础是解题关键,题目难度中等.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:实验题
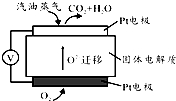 通过煤的气化和液化,使碳及其化合物得以广泛应用.
通过煤的气化和液化,使碳及其化合物得以广泛应用.| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 0.600 | 0.520 | 0.450 | 0.350 | 0.350 |
| n(CO)/mol | 0.400 | 0.320 | 0.250 | 0.150 | 0.150 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3:0.12 mol•L-1 | B. | H2O:0.09 mol•L-1 | ||
| C. | NO:0.03 mol•L-1 | D. | O2:0.15 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl的摩尔质量是58.5 g | |
| B. | 0.5 mol CO2气体中所含的CO2分子数约为3.01×1023 | |
| C. | 标准状况下,6.02×1022个CO2分子所占的体积约是22.4 L | |
| D. | 在1 L水中溶解5.85g NaCl,即可配制得0.1 mol•L-1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2的离子方程式:ClO-+CO2+H2O=HClO+HCO3- | |
| B. | 常温下用0.10 mol/L NaOH溶液分别滴定盐酸和醋酸溶液,以HA表示酸,当达到滴定终点时,两溶液中均存在c(Na+)=c(A-) | |
| C. | c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]<c(NH4Cl) | |
| D. | 1 mol冰醋酸和1mol乙醇在浓硫酸、加热条件下充分反应生成的水分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(3) | B. | (2)(4) | C. | (1)(2)(4)(6) | D. | (2)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
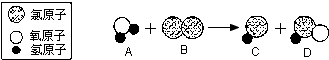
| A. | A物质属于氧化物 | |
| B. | D物质中氯元素的化合价为+1价 | |
| C. | 反应物和生成物均属于化合物 | |
| D. | 反应前后元素的种类和原子个数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(SiF4)消耗=4v(HF)生成 | B. | HF的体积分数不再变化 | ||
| C. | 容器内气体压强不再变化 | D. | 容器内气体的总质量不再变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com