
”¾ĢāÄæ”æÄ³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘĮĖŅ»×鏵ŃéŃéÖ¤ŌŖĖŲÖÜĘŚĀÉ£®
£Ø1£©¼×Ķ¬Ń§ŌŚa”¢b”¢cČżÖ»ÉÕ±Ąļ·Ö±š¼ÓČė50mLĖ®£¬ŌŁ·Ö±šµĪ¼Ó¼øµĪ·ÓĢŖČÜŅŗ£¬ŅĄ“Ī¼ÓČė“óŠ”Ļą½üµÄļ®”¢ÄĘ”¢¼Ųæ飬¹Ū²ģĻÖĻó£®¼×Ķ¬Ń§Éč¼ĘŹµŃéµÄÄæµÄŹĒ£»·“Ó¦×ī¾ēĮŅµÄŹĒ £®
£Ø2£©ŅŅĶ¬Ń§Éč¼ĘŹµŃéŃéÖ¤·Ē½šŹōŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌ¾ĶŌ½Ē森ĖūÉč¼ĘĮĖČēĶ¼×°ÖĆŅŌŃéÖ¤µŖ”¢Ģ¼”¢¹čŌŖĖŲµÄ·Ē½šŹōŠŌĒæČõ£® ŅŅĶ¬Ń§Éč¼ĘµÄŹµŃéæÉÖ±½ÓÖ¤Ć÷ČżÖÖĖįµÄĖįŠŌĒæČõ£¬ŅŃÖŖAŹĒĒæĖį£¬æÉÓėĶ·“Ó¦£»BŹĒæéד¹ĢĢ壻“ņæŖ·ÖŅŗĀ©¶·µÄ»īČūŗó£¬æÉ擵½ÓŠ“óĮæĘųÅŻD²śÉś£»ÉÕ±ÖŠæɹŪ²ģµ½°×É«³ĮµķCÉś³É£®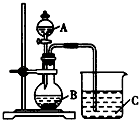
£Øi£©Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗA”¢C”¢D £®
£Øii£©Š“³öÉÕ±ÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ £®
£Øiii£©Ģ¼”¢µŖ”¢¹čČżÖÖŌŖĖŲµÄ·Ē½šŹōŠŌÓÉĒæµ½ČõĖ³ŠņĪŖ £®
£Øiv£©±ūĶ¬Ń§ČĻĪŖŅŅĶ¬Ń§Éč¼ĘµÄŹµŃé²»¹»ŃĻ½÷£¬Ó¦øĆŌŚBŗĶCÖ®¼äŌö¼ÓŅ»øöĻ“Ęų×°ÖĆ£¬øĆ×°ÖĆÖŠÓ¦Ź¢·Å£ØĢīŹŌ¼Į£©£®
”¾“š°ø”æ
£Ø1£©±Č½Ļļ®”¢ÄĘ”¢¼ŲµÄ½šŹōŠŌĒæČõ£»c
£Ø2£©HNO3£»Na2SiO3£»CO2£»CO2+SiO32©+H2OØTH2SiO3”ż+CO32©£»N£¾C£¾Si£»±„ŗĶNaHCO3
”¾½āĪö”æ½ā£ŗ£Ø1£©ÓÉ”°ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘĮĖŅ»×鏵ŃéŃéÖ¤ŌŖĖŲÖÜĘŚĀÉ”±æÉÖŖ£¬¼×Ķ¬Ń§Éč¼ĘŹµŃéµÄÄæµÄŹĒŃéÖ¤ļ®”¢ÄĘ”¢¼ŲµÄ½šŹōŠŌĒæČõ£» ½šŹōŠŌK£¾Na£¾Li£¬½šŹōŠŌŌ½Ē棬µ„ÖŹÓėĖ®·“Ó¦Ō½¾ēĮŅ£¬¹Ź·“Ó¦×ī¾ēĮŅµÄÉÕ±ŹĒC£¬ĖłŅŌ“š°øŹĒ£ŗ±Č½Ļļ®”¢ÄĘ”¢¼ŲµÄ½šŹōŠŌĒæČõ£»c£»£Ø2£©£Øi£©ĄūÓĆĒæĖįÖʱøČõĖį½ųŠŠ£¬AŹĒĒæĖį£¬³£ĪĀĻĀæÉÓėĶ·“Ó¦£¬ĻõĖį£»BŹĒæéד¹ĢĢ壬“ņæŖ·ÖŅŗĀ©¶·µÄ»īČūŗó£¬CÖŠæɹŪ²ģµ½°×É«³ĮµķÉś³É£¬ŌņBĪŖĢ¼ĖįøĘ”¢CĪŖ¹čĖįÄĘ£¬ĖłŅŌ“š°øŹĒ£ŗHNO3£»Na2SiO3£»CO2£»£Øii£©ÉÕ±ÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCO2+SiO32©+H2OØTH2SiO3”ż+CO32© £¬ ĖłŅŌ“š°øŹĒ£ŗCO2+SiO32©+H2O=CO32©+H2SiO3”ż£»£Øiii£©ŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌŌ½Ē棬ÓÉŹµŃéæÉÖŖĖįŠŌ£ŗĻõĖį“óÓŚĢ¼Ėį£¬Ģ¼Ėį“óÓŚ¹čĖį£¬Ōņ·Ē½šŹōŠŌ£ŗN£¾C£¾Si£»ĖłŅŌ“š°øŹĒ£ŗN£¾C£¾Si£»£Øiv£©ŅņĻõĖįŅ×»Ó·¢£¬ŌņÉś³ÉµÄ¶žŃõ»ÆĢ¼ĘųĢåÖŠ»ģÓŠĻõĖįÕōĘų£¬ŌņÓ¦ÓƱ„ŗĶĢ¼ĖįĒāÄĘ³żČ„ĻõĖį£¬ĖłŅŌ“š°øŹĒ£ŗ±„ŗĶNaHCO3 £®
”¾æ¼µć¾«Īö”æÕĘĪÕ·Ē½šŹōŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆ¼°ĘäŠŌÖŹµŻ±äµÄ¹ęĀÉŹĒ½ā“š±¾ĢāµÄøł±¾£¬ŠčŅŖÖŖµĄŌŚÄæĒ°ŅŃÖŖµÄ112ÖÖŌŖĖŲÖŠ£¬·Ē½šŹōŌŖĖŲÓŠ22ÖÖ£¬³żHĶā·Ē½šŹōŌŖĖŲ¶¼Ī»ÓŚÖÜĘŚ±ķµÄÓŅÉĻ·½£ØHŌŚ×óÉĻ·½£©£®FŹĒ·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ25”ꏱ£¬Ļņ100mLŗ¬HCl 14.6gµÄŃĪĖįÖŠ£¬·ÅČė5.6gĢś·Ū£¬·“Ó¦½ųŠŠµ½2sŹ±ŹÕ¼Æµ½ĒāĘų1.12L£Ø±ź×¼×“æö£©£¬Ö®ŗó·“Ó¦ÓÖ½ųŠŠĮĖ4s£¬Ģś·ŪČ«Čܽā£®Čō²»æ¼ĀĒĢå»ż±ä»Æ£¬Ōņ£ŗ
£Ø1£©Ē°2sÄŚÓĆFeCl2±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ
£Ø2£©ŗó4sÄŚÓĆHCl±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ
£Ø3£©Ē°2sÓėŗó4s±Č½Ļ£¬·“Ó¦ĖŁĀŹ½Ļæģ£¬ĘäŌŅņæÉÄÜ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪŽÉ«ČܹöÖŠæÉÄÜŗ¬ÓŠNa+”¢NH4+”¢Ba2+”¢Cu2+”¢SO42©”¢SO32©”¢Cl©”¢Br©”¢CO32©ÖŠµÄČōøÉÖÖ£®ĪŖ¼ģŃéĘäÖŠŗ¬ÓŠµÄĄė×Ó£¬½ųŠŠČēĻĀŹµŃé£ŗ
¢ŁČ”10mLČÜŅŗ£¬¼ÓČė×ćĮæĀČĖ®£¬£®ĪŽĘųĢå²śÉś£¬ŌŁ¼ÓČėCCl4ČÜŅŗ·Ö²ć£¬ĻĀ²ćĪŖ³ČŤɫ£»
¢Ś·ÖŅŗŗ󣬽«¢ŁÖŠÉĻ²ćČÜŅŗ¼ÓČė×ćĮæBaCl2ŗĶHClČÜŅŗ£¬²śÉś°×É«³Įµķ2.33g£»
¢ŪĮķČ”10mLŌČÜŅŗ£¬¼ÓČė¹żĮæµÄÅØĒāŃõ»ÆÄĘČÜŅŗ²¢¼ÓČČ£¬ŹÕ¼Æµ½±ź×¼×“æöĻĀ448mĘųĢ壮ĻĀĮŠ¹ŲÓŚŌČÜŅŗµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.æĻ¶Ø“ęŌŚNH4+”¢Cl©”¢Br©
B.SO42©”¢SO32©ÖĮÉŁŗ¬ÓŠŅ»ÖÖ
C.ŹĒ·ń“ęŌŚNa+ŠčŅŖĶعżŃęÉ«·“Ó¦Ą“Č·¶Ø
D.æĻ¶Ø²»“ęŌŚBa2+”¢Cu2+”¢SO32©”¢CO32©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¬Ö÷×åŌŖĖŲŠĪ³ÉµÄĶ¬Ņ»ĄąŠĶµÄ»ÆŗĻĪļ£¬ĶłĶł½į¹¹ŗĶŠŌÖŹŗÜĻąĖĘ£¬ČēPH4IµÄ½į¹¹ŗĶŠŌÖŹÓėNH4ClĻąĖĘ£¬ÓŠ¹Ų¶ŌPH4IµÄŠšŹöÖŠ²»ÕżČ·µÄŹĒ£Ø £©
A£®æÉÓÉPH3ÓėHI»ÆŗĻÉś³É B£®½«Ęä¼ÓČČæÉŅŌ·Ö½ā
C£®ÄÜøśNaOHČÜŅŗ·“Ó¦ D£®ŹĒŅ»ÖÖ¹²¼Ū»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ( )
A.ŗ¬ÓŠōĒ»łµÄÓŠ»śĪļ³ĘĪŖ“¼
B.ÄÜ·¢ÉśŅų¾µ·“Ó¦µÄÓŠ»śĪļ¶¼ŹĒČ©
C.±½·ÓĖ×³ĘŹÆĢæĖį£¬ĖįŠŌ±ČĢ¼ĖįĒæ
D.C3H6ŗĶC4H8²»Ņ»¶ØŹĒĶ¬ĻµĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹śČżĻ湤³ĢĖłĢį¹©µÄĖ®µē£¬Ļąµ±ÓŚĆæÄźČ¼ÉÕ3000Ķņ¶ÖŌĆŗµÄ»šĮ¦·¢µēÕ¾²śÉśµÄµēÄÜ£¬Ņņ“ĖČżĻ湤³ĢÓŠÖśÓŚæŲÖĘ
A. Ė®ĢåĪŪČ¾B. °×É«ĪŪČ¾C. ĖįÓź²śÉśD. Å©Ņ©”¢»Æ·ŹĪŪČ¾
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĢāŅā½ā“š
£Ø1£©Ä³ĪĀ¶ČŹ±£¬2LµÄĆܱÕČŻĘ÷ÖŠX”¢Y”¢Z=ÖÖĘųĢåĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĶ¼ ĖłŹ¾£® 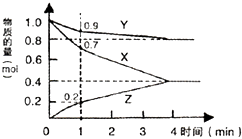
ÓÉĶ¼ÖŠŹż¾Ż·ÖĪö£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ØÓĆX”¢Y”¢Z±ķŹ¾£©£¬·“Ó¦æŖŹ¼ÖĮ1min£¬XµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £® Čō4minŹ±·“Ó¦“ļµ½×ī“óĻŽ¶Č£¬ZµÄĪļÖŹµÄĮæµČÓŚ0.4 mol£®“ĖŹ±£¬XµÄ×Ŗ»ÆĀŹĪŖ £¬ YµÄĪļÖŹµÄĮæÅضČĪŖ
£Ø2£©æÉÄę·“Ó¦£ŗ2NO2£Øg£©2NO£Øg£©+O2£Øg£©£¬ŌŚĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ£ØĢīŠņŗÅ£©£® ¢Łµ„Ī»Ź±¼äÄŚÉś³ÉnmolO2µÄĶ¬Ź±Éś³É2nmolNO2
¢Śµ„Ī»Ź±¼äÄŚÉś³ÉnmolO2µÄĶ¬Ź±Éś³É2nmolNO
¢ŪÓĆNO2”¢NO”¢O2µÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹµÄ±ČĪŖ2£ŗ2£ŗ1µÄדĢ¬
¢Ü»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁøıäµÄדĢ¬
¢Ż»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøıäµÄדĢ¬£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČ”ÄĘ©Ć¾ŗĻ½š7.0æĖ½ųŠŠČēĻĀŹµŃé£ŗ 
£Ø1£©Š“³öMgŌŚCO2ÖŠČ¼ÉյĻÆѧ·½³ĢŹ½
£Ø2£©ĻņČÜŅŗ1ÖŠ¼Ó¹żĮæµÄNaOHČÜŅŗ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ
£Ø3£©Š“³öŗĻ½šµÄ»Æѧ×é³É £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆѧ¹żµÄ»ÆѧÖŖŹ¶½ā“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĻĀĮŠ·“Ó¦ÖŠ£¬ŹōÓŚĪüČČ·“Ó¦µÄŹĒ£ØĢīŠņŗÅ£©£® ¢ŁģŃÉÕŹÆ»ŅŹÆ”” ¢ŚÄ¾ĢæČ¼ÉÕ”” ¢ŪÕØŅ©±¬ÕØ ””¢ÜĖį¼īÖŠŗĶ
¢ŻÉśŹÆ»ŅÓėĖ®×÷ÓĆÖĘŹģŹÆ»Ņ”” ¢ŽŹ³ĪļŅņŃõ»Æ¶ųøÆ°Ü
£Ø2£©ÓĆĶ”¢ŅųÓėĻõĖįŅųÉč¼ĘŅ»øöŌµē³Ų£¬“Ėµē³ŲµÄÕż¼«ŹĒ £¬ øŗ¼«µÄµē¼«·“Ó¦Ź½ŹĒ £®
£Ø3£©ÓĆŠæʬ”¢ĶʬĮ¬½Óŗó½žČėĻ”ĮņĖįČÜŅŗÖŠ£¬¹¹³ÉĮĖŌµē³Ų£¬¹¤×÷Ņ»¶ĪŹ±¼ä£¬ŠæʬµÄÖŹĮæ¼õÉŁĮĖ3.25g£¬Ķ±ķĆęĪö³öĮĖĒāĘųL£Ø±ź×¼×“æö£©£¬µ¼ĻßÖŠĶعżmolµē×Ó£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com