
【题目】配制一定物质的量浓度的稀盐酸,结果偏高的是
A. 在容量瓶中定容时,俯视刻度线
B. 用量筒量取浓盐酸时,俯视刻度线
C. 转移溶液后,未洗涤烧杯和玻璃棒就直接定容
D. 定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】关于合金性质的说法中,错误的是( )
A. 合金的硬度一般比其各成分金属的硬度高
B. 合金的熔点一般比其各成分金属的熔点低
C. 合金的物理性质一般与其各成分金属的的物理性质不同
D. 合金的化学性质一般与其各成分金属的的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行实验探究:探究碳、硅元素的非金属性的相对强弱.实验装置如下,请根据要求回答下列问题:
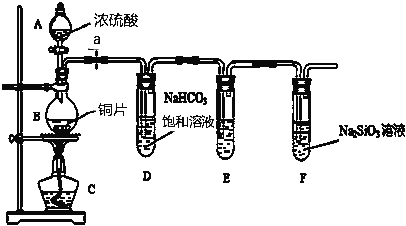
(1)填写所示仪器名称A____________
(2)实验步骤:连接仪器、__________________、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是_________________________________________________.
装置E中盛足量酸性KMnO4溶液的作用是__________________________.
②该实验证明碳元素的非金属性比硅元素非金属性强的实验依据是__________________.
请写出F 中发生反应的离子方程式________________________.
③依据试管D中的发生的反应,能否证明硫元素的非金属性强于碳元素的非金属性______(填“能”或“否”),原因是_______________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、写出下列化合物的名称或结构简式:
①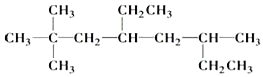 的名称为________________________.
的名称为________________________.
②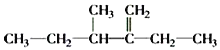 的名称为______________________________.
的名称为______________________________.
II、已知有机化合物X中各元素的质量分数分别为C---60%,H---13.3%,O---26.7%。
请填空:
(1)有机物X的实验式为____________。若0.1molX在足量氧气中充分燃烧需消耗氧气10.08L(标准状况),则X的分子式为________。
(2)实验表明:X能与金属钠反应产生H2。X分子的核磁共振氢谱中有4个吸收峰,且面积之比为3:2:2:1,则X分子中含有的官能团的名称为_________,X的结构简式为_____________。
(3)X有两种同分异构体Y和Z,其中Y能与金属钠反应产生H2,而Z不能。则Y、Z的结构简式分别为_______________、_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4和H2O在一定条件下, 可以转化为合成一系列有机化合物、氨的重要原料(CO+H2),这种方法称作甲烷水蒸气重整法制合成气,其能量变化如图:

(1)甲烷水蒸气重整法制合成气的热化学方程式为_______;该反应只有在_____(填“高温”、“低温”或“常温”)才自发进行。
(2)下列有关甲烷水然气重整法制合成气的说法正确的是_____(填字母)。
A.相同条件下,该反应的逆反应更易发生
B.恒温恒容时充入一定量CO2,可促进CH4转化并可调节CO和H2的比例
C.若反应的高效催化剂为A,则A一定是CO和H2合成CH4的高效催化剂
D.恒温时向上述平衡体系中充入少量Ar,平衡一定不移动
E.有副反应:H2O+CO![]() CO2+H2
CO2+H2
(3)在恒容密闭容器中充入2mol的CH4和H2O(g)混合气体,且CH4和H2O(g)的物质的量之比为x,相同温度下测得H2平衡产率与x的关系如图所示。请问a、b两点比较(填“>”、“<”、“=”);CH4的转化率a点____b点,a点CH4的浓度_____b点H2O(g)的浓度,氢气的产率a点_____b点。

(4)当充入CH4和H2O(g)物质的量之比1:2.2时,温度、压强p对平衡时CO体积分数φ(CO)的影响如图,则压强由大到小的排序是_____;当T<450℃和T≥1000℃时,压强p对φ(CO)几乎无影响的原因是_____________________。
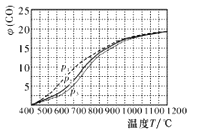
(5)在下图左室充入1molCH4和H2O(g)混合气体(物质的量之比为1:1),恒温条件下反应建立平衡,测得CH4的转化率为50%,则其平衡常数为_________ 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事。这个先后顺序跟下列有关的是:①地壳中的金属元素的含量②金属活动性③金属的导电性 ④金属冶炼的难易程度 ⑤金属的延展性
A. ①③ B. ②⑤ C. ③⑤ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在MgCl2、KCl、K2SO4三中盐的混合溶液中,若K+、Cl—、Mg2+的物质的量分别为1.5mol、1.5mol、0.5mol,则SO42—的物质的量为( )
A. 0.1mol B. 0.15mol C. 0.5mol D. 0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许 Li+通过,电池反应式
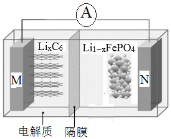
为LixC6+Li1-xFePO4 ![]() LiFePO4+6C。下列说法正确的是
LiFePO4+6C。下列说法正确的是
A.放电时Li+从右边移向左边
B.放电时M是负极,电极反应式为:C6x--xe-=6C
C.充电时N极连接电源的正极,电极反应式为:LiFePO4-xe-=Li1-xFePO4+xLi+
D.充电时电路中通过0.5mol电子,消耗36gC
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com