
| A£® | ÅÅĖ®·ØŹÕ¼ÆĘųĢåŗó£¬ĻČĻØĆš¾Ę¾«µĘ£¬ŌŁČ”³öµ¼Ęų¹Ü | |
| B£® | ÕōĮó×ŌĄ“Ė®Ź±£¬ĄäÄżĖ®“ÓÉĻæŚ½ų£¬“ÓĻĀæŚ³ö | |
| C£® | ÓĆŹŌ¹ÜČ”³öŹŌ¼ĮĘæÖŠµÄNa2CO3ČÜŅŗ£¬·¢ĻÖČ”Įæ¹ż¶ą£¬ĪŖĮĖ²»ĄĖ·Ń£¬ÓÖ°Ń¹żĮæµÄŹŌ¼Įµ¹ČėŹŌ¼ĮĘæÖŠ | |
| D£® | Ļ”ŹĶÅØĮņĖįŹ±£¬Ó¦½«ÅØĮņĖįĀżĀż¼ÓČėĖ®ÖŠ²¢¼°Ź±½Į°č |
·ÖĪö A£®ŅŖĻČ“ÓĖ®²ŪÖŠ³·³öµ¼Ęų¹Ü£¬ŌŁĻØĆš¾Ę¾«µĘ£»
B£®ĄäÄż¹ÜÖŠÓ¦øĆ²ÉÓĆÄęĻņĶØĖ®£¬ĄäÄżŠ§¹ū½ĻŗĆ£»
C£®ŹµŃé¹ż³ĢÖŠŹ£ÓąŅ©Ę·Ņ»°ć²»ÄÜ·Å»ŲŌŹŌ¼ĮĘ棬·ńŌņČŻŅ×ĪŪČ¾ŹŌ¼Į£»
D£®Ļ”ŹĶÅØĮņĖįŹ±£¬ÅØĮņĖįµÄĆܶȓóÓŚĖ®£¬Ó¦½«ÅØĮņĖįµ¹ČėĖ®ÖŠ£®
½ā“š ½ā£ŗA£®ÓĆÅÅĖ®·ØŹÕ¼ÆŃõĘųµÄŹµŃé½įŹųŹ±£¬ŅŖĻČ“ÓĖ®²ŪÖŠ³·³öµ¼Ęų¹Ü£¬ŌŁĻØĆš¾Ę¾«µĘ£¬ÕāŹĒĪŖĮĖ·ĄÖ¹Ė®²ŪÄŚµÄĖ®ŌŚ“óĘųŃ¹ĒæµÄ×÷ÓĆĻĀ£¬Ė³×ŵ¼¹Üµ¹½ųČėČČŹŌ¹Üµ×²æŹ¹ŹŌ¹ÜÕØĮŃ£¬¹ŹA“ķĪó£»
B£®ÕōĮó×ŌĄ“Ė®Ź±£¬Ó¦øĆ²ÉÓĆÄęĻņĶØĖ®£¬¼“ĄäÄżĖ®“ÓĻĀæŚ½ų£¬“ÓÉĻæŚ³ö£¬¹ŹB“ķĪó£»
C£®ŹµŃéŗóŹ£ÓąµÄŅ©Ę·£¬Ó¦øƵ¹Čė·ĻŅŗ³M£¬²»ÄÜ·Å»ŲŌŹŌ¼ĮĘæÖŠ£¬·ńŌņ»įĪŪČ¾Ņ©Ę·£¬¹ŹC“ķĪó£»
D£®Ļ”ŹĶÅØĮņĖįŹ±£¬ÓÉÓŚÅØĮņĖįĆÜ¶Č½Ļ“ó£¬ĒŅøĆ·“Ó¦·Å³ö“óĮæČČ£¬Ó¦½«ÅØĮņĖįĀżĀż¼ÓČėĖ®ÖŠ²¢¼°Ź±½Į°č£¬Ė³Šņ²»Äܵߵ¹£¬±ÜĆā·¢ÉśĪ£ĻÕ£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆѧŹµŃé·½°øµÄĘĄ¼Ū£¬ĢāÄæÄŃ¶Č²»“ó£¬Éę¼°ÕōĮó”¢ÅØĮņĖįĻ”ŹĶ”¢»ÆѧŹµŃé²Ł×÷µČÖŖŹ¶£¬Ć÷Č·»ÆѧŹµŃ黳±¾²Ł×÷·½·ØĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°»ÆѧŹµŃéÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SO4ŗĶBa£ØOH£©2 | B£® | CO2ŗĶNaOH | C£® | CaCO3ŗĶHCl | D£® | Mg£ØOH£©2ŗĶCuSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 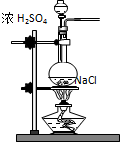 | B£® | 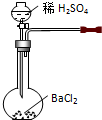 | C£® | 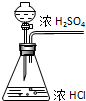 | D£® | 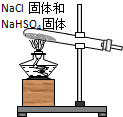 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øƵē³ŲµÄµēĮ÷·½ĻņŹĒÓÉŠæµ½¶žŃõ»ÆĆĶ | |
| B£® | øƵē³Ų·“Ó¦ÖŠMnO2Ęš“ß»Æ×÷ÓĆ | |
| C£® | µ±0.1molZnĶźČ«ČܽāŹ±£¬Į÷¾µē½āŅŗµÄµē×ÓøöŹżĪŖ1.204”Į1023 | |
| D£® | µē³ŲÕż¼«·“Ó¦ĪŖMnO2+e-+H2OØTMnO£ØOH£©+OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 +Br2”ś
+Br2”ś £»
£» £»
£» £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com