
 2NO2(正反应是放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
2NO2(正反应是放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )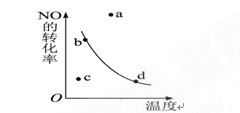
| A.a | B.b | C.c | D.d |
科目:高中化学 来源:不详 题型:单选题
| A.K值越大,正反应进行的程度越大 |
| B.一般地说,K>105时,该反应进行得就基本完全了 |
| C.压强越大,K值越大 |
| D.K与反应物或生成物的浓度变化无关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 eC(g)+fD(g)在反应过程中,当其他条件不变时,C的体积分数
eC(g)+fD(g)在反应过程中,当其他条件不变时,C的体积分数 (C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是 ( )
(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是 ( )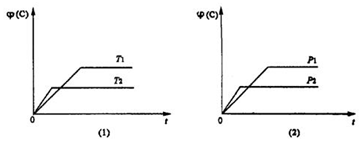
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是| A.容器内压强不随时间变化 | B.V正(X)=2V逆(Z) |
| C.容器内X、Y、Z的浓度相等 | D.容器内气体密度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2 HX(g)的平衡常数为64,将2 mol H2和2 mol X2通入体积为1L的密闭容器中,该温度下H2的平衡转化率为
2 HX(g)的平衡常数为64,将2 mol H2和2 mol X2通入体积为1L的密闭容器中,该温度下H2的平衡转化率为| A.20﹪ | B.40﹪ | C. 60﹪ | D.80﹪ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.该反应已停止 |
| B.单位时间内氮气的消耗速率等于氢气的生成速率 |
| C.3v(H2)=2v(NH3) |
| D.c(H2) :c(N2) :c(NH3) =" 7" :9 :2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 nY(g);ΔH =QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g);ΔH =QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示: 温度℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.09 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Ag+(aq)+Cl-(aq) 在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol·L-1 AgNO3溶液 ③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为__________________(填序号),此时溶液②中Cl-物质的量浓度为__________________。
Ag+(aq)+Cl-(aq) 在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol·L-1 AgNO3溶液 ③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为__________________(填序号),此时溶液②中Cl-物质的量浓度为__________________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com