
 �ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ͼ��ʾ��ת����ϵ������������ͷ�Ӧ������ȥ����
�ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ͼ��ʾ��ת����ϵ������������ͷ�Ӧ������ȥ����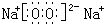 ��DΪ��ɫ��������ΪAl��OH��3����BΪNaOH��EΪO2��XΪ����Al3+��CΪNaAlO2��C��X��Ӧ�����ӷ���ʽΪ3AlO2-+Al3++6H2O=4Al��OH��3����
��DΪ��ɫ��������ΪAl��OH��3����BΪNaOH��EΪO2��XΪ����Al3+��CΪNaAlO2��C��X��Ӧ�����ӷ���ʽΪ3AlO2-+Al3++6H2O=4Al��OH��3����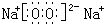 ��3AlO2-+Al3++6H2O=4Al��OH��3����
��3AlO2-+Al3++6H2O=4Al��OH��3����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��13 | B��14 |
| C��15 | D������ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ԣ�A��B |
| B��A�����������������Һ���������� |
| C��B���Ǹ��� |
| D��Ҫ�ж�A����B�����������Ǹ��������迼�ǵ������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ̼���γɻ�������������Ԫ�أ��䵥�ʼ������������������������Ҫ��Դ���ʣ���ش��������⣺
̼���γɻ�������������Ԫ�أ��䵥�ʼ������������������������Ҫ��Դ���ʣ���ش��������⣺| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||||
| B��CH4��C2H6 | ||||
| C�����������춡�� | ||||
| D����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij������Һ��������������ӣ������Һ�Լ��ԣ�ֻ�����ᷴӦ |
| B���Һͼ���ͬ��Ԫ�ص�����������ȣ�������ʹʪ���KI������ֽ���� |
| C�����к��Т�A��Ԫ�أ�����ͬ�����±��ȼ��ȶ� |
| D�������ķ�����ɷ���XY3�ͽṹ�����Ӽ������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com