
| A. | CH3CH(CH3)CH(CH3)2的系统名称是2,3一二甲基丁烷 | |
| B. | 石油化工中裂化是为了提高轻质油的产量和质量 | |
| C. | 维勒在制备氰酸铰时得到了尿素,打破了“生命力论”的统治地位 | |
| D. | 乙醇和浓硫酸加热到170°时发生脱水生成乙醚 |
分析 A.选取碳原子最多的碳链为主碳链,离取代基近的一端编号确定取代基位置,写出名称判断;
B.石油裂化的目的主要是提高汽油的产量;
C.德国化学家维勒首次人工合成尿素,首次用无机物人工合成有机物;
D.将乙醇和浓硫酸反应的温度控制在170℃,生成乙烯;
解答 解:A.CH3CH(CH3)CH(CH3)2的最长碳链含四个碳原子,离取代基近的一端编号,系统命名法得到名称是2,3一二甲基丁烷,故A正确;
B.石油裂化的目的为了提高轻质液体燃料(汽油,煤油,柴油等)的产量,特别是提高汽油的产量,故B正确;
C.德国化学家维勒首次人工合成尿素,首次用无机物人工合成有机物,彻底动摇了“生命力论”,故C正确;
D.将乙醇和浓硫酸反应的温度控制在170℃,生成乙烯,而加热到140℃时,可生成乙醚,故D错误;
故选D.
点评 本题考查了有机物命名、石油裂化、乙醇性质等知识点,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O≡C=O | N2/N≡N |
| 化学键 | N≡O | C≡O | C≡O | N≡N |
| 键能(kJ/mol) | 632 | 1072 | 750 | 946 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/×10-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n(NO)/×10-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 酚酞不能用作本实验的指示剂 | |
| B. | 盐酸的物质的量浓度为1mol?L-1 | |
| C. | P点时恰好完全中和,溶液呈中性 | |
| D. | 曲线a是盐酸滴定氢氧化钠溶液的滴定曲线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Fe2+、NO3-、Cl-- | B. | K+、Al3+、SO42-、Cl- | ||
| C. | K+、NH4+、SO42-、Cl- | D. | Na+、K+、Br-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
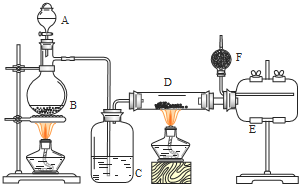 无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.
无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{1}$He | B. | ${\;}_{2}^{3}$He | C. | ${\;}_{2}^{5}$He | D. | ${\;}_{2}^{1}$He |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com