
| A�� | ��˫��ˮ���������������� | |
| B�� | �ö�����������������ʵ�� | |
| C�� | ����ˮ�����ˮ������ȡʵ�� | |
| D�� | ��ͭ�۴���ͭ˿����ͭ��Ũ����ķ�Ӧ |
���� ��ɫ��ѧ������ص��Ǵ�Դͷ�Ͳ���Ԥ����Ⱦ�Ŀ�ѧ�ֶΣ�������̺��ն˾�Ϊ���ŷŻ�����Ⱦ���ݴ˼��ɽ��
��� �⣺A��2H2O2$\frac{\underline{\;MnO_{2}\;}}{��}$2H2O+O2����2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2�����ù�������Ͷ���������ȡ���������ø�������ڼ�������ȡ������ȣ�������ȣ���Լ��Դ��������������ˮ��û����Ⱦ��ת�����������еIJ�Ʒ��ʵ������ɫ��ѧ�������A��ȷ��
B��Cl2���ж�����֮һ���ʲ�������ɫ��ѧ�����B����
C����ˮ�ӷ����������ж����ʲ�������ɫ��ѧ�����C����
D��ͭ˿����Cu��Ũ����ķ�Ӧ�����Կ��Ʒ�Ӧ���ʣ���Ũ�������Ƴ�ͭ˿��Ӧ�ͻ�ֹͣ����ͭ�������Ʒ�Ӧ���ʣ���������ɫ��ѧ�������D����
��ѡA��
���� �����㿼������ɫ��ѧ��������ɫ��ѧ�ĸ����ǽ��Ĺؼ�����Ŀ�ѶȲ���


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100 mL | B�� | 200 mL | C�� | 300 mL | D�� | 400 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
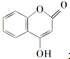 ��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�
��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�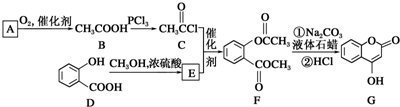
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCOOH | B�� | HOOC-COOH | C�� | HOCH2CH2COOH | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2mol SO2��1mol O2��һ�������³�ַ�Ӧ�����û������ķ�����С��2NA | |
| B�� | ��1mol CH3COONa������CH3COOH�γɵ�������Һ�У�CH3COO-��ĿΪNA�� | |
| C�� | ���³�ѹ�£�14g��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪNA | |
| D�� | ��״���£�6.72L NO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeS��Ksp��CuS��Ksp | |
| B�� | �ﵽƽ��ʱc��Fe2+��=c��Cu2+�� | |
| C�� | �÷�Ӧƽ�ⳣ��K=$\frac{{K}_{sp}��FeS��}{{K}_{sp}��CuS��}$ | |
| D�� | ��Һ�м�������Na2S�������Һ��c��Cu2+����c��Fe2+�����ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ӿ�ʼ��ƽ��A��ƽ����Ӧ����Ϊ0.3mol/��Ls�� | |
| B�� | �ӿ�ʼ��ƽ��B��ת����Ϊ60% | |
| C�� | �˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=$\frac{c��C��•{c}^{2}��D��}{{c}^{3}��A��•c��B��}$ | |
| D�� | �����������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | I A | ��A | ��A | ��A | ��A | ��A | ��A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
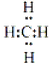 ��
��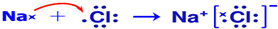
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
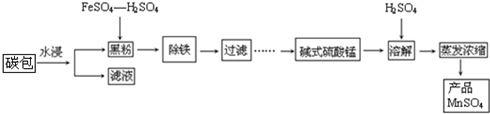
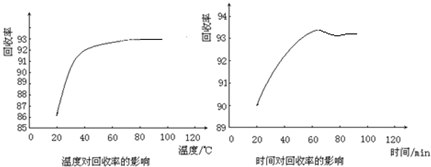
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com