
【题目】化学与社会、生产、生活密切相关,下列说法正确的是
A.氢氧化铝、氢氧化钠都是常见的胃酸中和剂
B.海轮外壳镶嵌锌块是利用牺牲阳极的阴极保护法
C.水泥、玛瑙、分子筛都是硅酸盐工业产品
D.明矾净水时的作用是杀菌、消毒
科目:高中化学 来源: 题型:
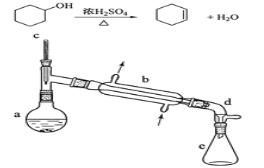
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
可能用到的有关数据如下:
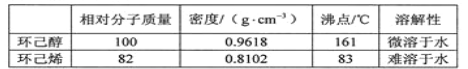
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。B中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置b的名称是 。
(2)加入碎瓷片的作用是 ;如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作时 (填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为 。
(4)分液漏斗在使用前须清洗干净并 ;在本实验分离过程中,产物应该从分液漏斗的 (填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是 。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有 (填正确答案标号)。
A.蒸馏烧瓶
B.温度计
C.吸滤瓶
D.球形冷凝管
E.接收器
(7)本实验所得到的环己烯产率是 (填正确答案标号)。
A.41% B.50% C.61% D.70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3 mol·L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
A. 开始加入合金的质量可能为3.6g
B. 参加反应的硝酸的物质的量为0.1mol
C. 沉淀完全时消耗NaOH溶液的体积为100mL
D. 溶解合金时产生NO的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸铵广泛应用与工农生产中,其生产流程图如下,回答下列问题:
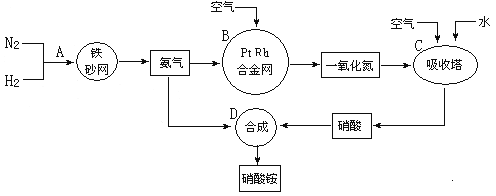
(1)在上述工业制硝酸的生产中,B设备的名称是 ,在反应中的氧化产物是 。
(2)此生产过程中,N2与H2合成NH3所用的催化剂是 。在合成氨的设备(合成塔)中,设置热交换器的目的是 ;在合成硝酸的吸收塔中通入空气的目的是 。
(3)科学家以氨(NH3)为燃料开发新型的燃料电池。电池中填充可传导O2—离子的 MnO3固体电解质,电池总反应为:4NH3+3O2=2N2+6H2O。负极的电极反应式为 。
(4)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量约占总耗NH3质量(不考虑其它损耗)的 %。(取两位有效数字)
(5)硝酸铵是一种常用的氮肥,在使用该化肥时避免与碱性肥料一起使用,理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是
编号 | 金属(粉末状) | 酸的浓度 | 酸的体积 | 反应温度 |
A | 0.1mol Mg | 6mol/L硝酸 | 10mL | 60℃ |
B | 0.1mol Mg | 3mol/L盐酸 | 10mL | 30℃ |
C | 0.1mol Fe | 3mol/L盐酸 | 10mL | 60℃ |
D | 0.1mol Mg | 3mol/L盐酸 | 10mL | 60℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①C(s)+1/2O2(g)=CO(g); △H=-110.5 kJ·mol-1
②C(s)+O2(g)=CO2(g) ; △H=-393.51 kJ·mol-1
则反应C(s)+CO2(g)=2CO(g)的△H为
A.-283.01 kJ·mol-1
B.+172.51 kJ·mol-1
C.+283.01 kJ·mol-1
D.-172.51 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的最外层电子的电子排布图________________________。
(2)根据元素周期律,原子半径Ga______As,第一电离能Ga_____As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol1和MAs g·mol1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
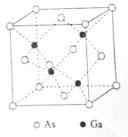
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝用途广泛,用铝土矿(主要成分为Al2O3·nH2O、少量SiO2和Fe2O3)制取Al有如下途径:

(1)滤液A可用于净水,其净水原理用离子方程式表示为_________________。
(2)灼烧时盛放药品的仪器名称是______________
(3)步骤Ⅴ中发生反应的化学方程式是________________________。
(4)步骤Ⅲ中生成固体C的离子反应方程式为__________________________。
(5)取滤液B 100 mL,加入1 mol/L盐酸200 mL,沉淀量达到最大且质量为11.7 g。则滤液B中c(Al O2-)=_____________。(4分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如下:
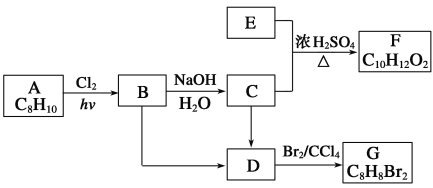
请回答下列问题:
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为 。
(2)A为一取代芳香烃,B中含有一个甲基。由B生成C的化学方程式为______________。
(3)由B生成D的反应条件是 ;由C生成D的反应类型是 。
(4)F存在于栀子香油中,其结构简式为________________________。
(5)在G的同分异构体中,苯环上一硝化的产物只有一种的共有 种,其中核磁共振氢谱有两组峰,且峰面积比为1∶1的是___________________(填结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com